Τι συμβαίνει σε ένα αέριο όταν αυξάνεται η πίεσή του;
Πόσο ωραίο είναι να αλλάζεις την κατάστασή σου;
Παγώστε με? Είμαι πάγος.
Θερμάτε με. Είμαι το νερό.
Βράστε με? Είμαι ο ατμός.
Έχω διαφορετικές μορφές και καταστάσεις:Είμαι Ύλη!
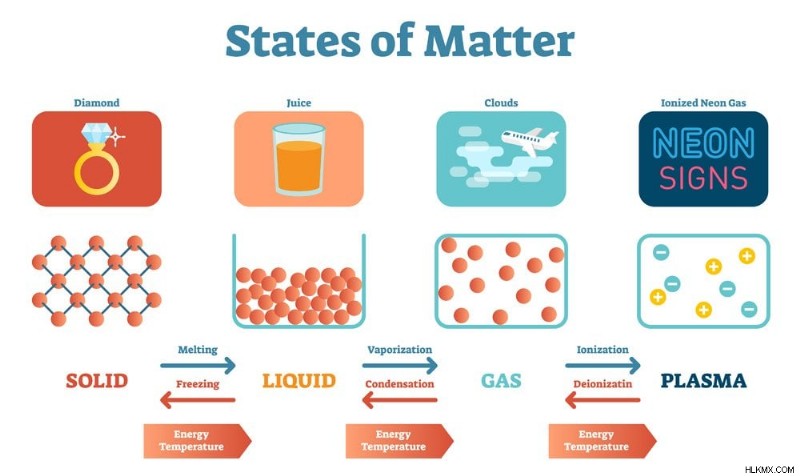
Οι διαφορετικές καταστάσεις της ύλης (Φωτογραφία :VectorMine/Shutterstock)
Η ευελιξία του 'Matter'
Με απλά λόγια, ο ορισμός της ύλης είναι κάτι που μεταφέρει μάζα και καταλαμβάνει χώρο.
Υπάρχουν τέσσερις θεμελιώδεις καταστάσεις της ύλης:Στερεό, Υγρό, Αέριο και Πλάσμα.
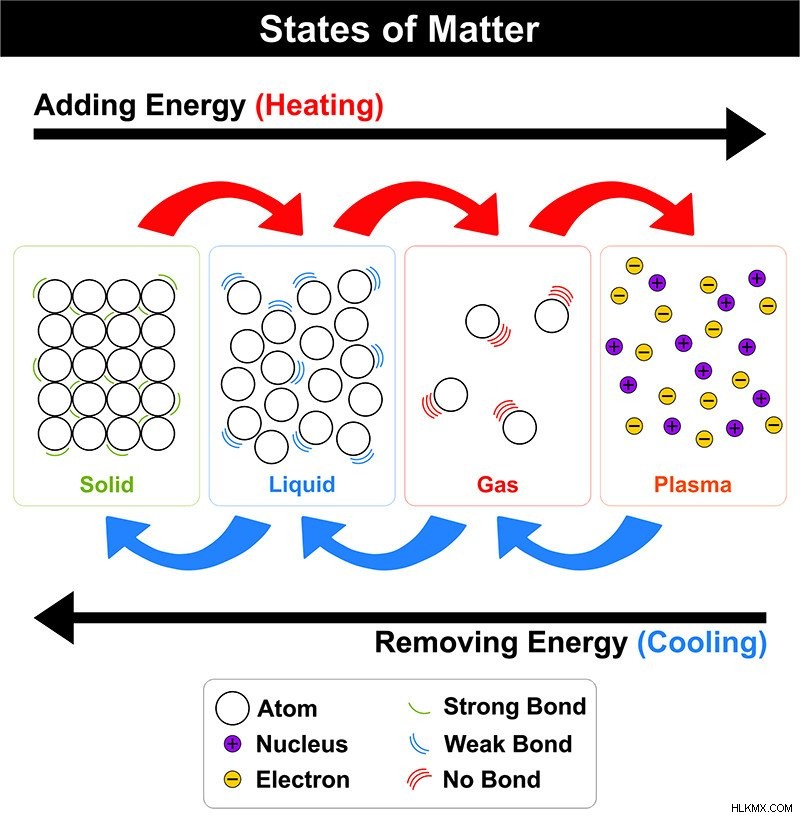
Διάταξη μορίων σε διαφορετικές καταστάσεις ύλης (Φωτογραφία :udaix/Shutterstock)
Στερεά:
Αυτά είναι άκαμπτα και ασυμπίεστα με συγκεκριμένο σχήμα και όγκο. Ισχυρές διαμοριακές δυνάμεις συγκρατούν τα μόρια μαζί με καθόλου ή αμελητέους διαμοριακούς χώρους. Τα μόρια στα στερεά έχουν χαμηλή κινητική ενέργεια και χαμηλή δονητική ενέργεια. Τα στερεά μπορούν να υπάρχουν σε δύο μορφές:κρυσταλλικά ή άμορφα.
Ο στερεός άνθρακας υπάρχει σε κρυσταλλική μορφή ως διαμάντι και σε άμορφη μορφή ως κάρβουνο.
Υγρά:
Αυτά είναι ρευστά, έχουν καθορισμένο όγκο, δεν έχουν καθορισμένο σχήμα (παίρνουν το σχήμα του δοχείου) και είναι ασυμπίεστα. Μέτριες διαμοριακές δυνάμεις συγκρατούν τα μόρια μαζί με ασθενείς διαμοριακούς χώρους. Τα μόρια στο υγρό κινούνται με μέτρια κινητική ενέργεια. Τα υγρά έχουν ιδιότητες τριχοειδούς δράσης, ιξώδους και επιφανειακής τάσης.
Αέρια:

Διαμοριακά διαστήματα στα αέρια (Φωτογραφία :Arisa_J/Shutterstock)
Αυτά είναι επίσης εξαιρετικά ρευστά, έχουν αόριστο σχήμα και όγκο και είναι εύκολα συμπιέσιμα. Οι διαμοριακές δυνάμεις σε ένα αέριο είναι πολύ αδύναμες και οι διαμοριακές αποστάσεις μεγάλες. Έτσι, τα αέρια ρέουν ελεύθερα και τα μόρια ενός αερίου κινούνται με υψηλή κινητική ενέργεια.
Πλάσμα:
Η πιο άφθονη κατάσταση της ύλης στο σύμπαν είναι το πλάσμα ή η υπερθερμασμένη ύλη.Το 99% της ύλης στο Σύμπαν βρίσκεται σε κατάσταση πλάσματος. Όταν η ενέργεια διέρχεται από ουδέτερο αέριο, τα ηλεκτρόνια απομακρύνονται για να σχηματίσουν θετικά και αρνητικά φορτισμένα ιόντα. Δεν έχει ούτε σχήμα ούτε όγκο. Το πλάσμα αποτελείται από τον ήλιο και τα αστέρια.

(Φωτογραφία:Quardia/Shutterstock)
Τι καθορίζει την κατάσταση της Ύλης;
Η ύλη έχει μια συγκεκριμένη κατάσταση σε μια δεδομένη θερμοκρασία και πίεση. Οι δύο παράγοντες που ρυθμίζουν την κατάστασή του είναι:
- Θερμοκρασία (εξηγείται από τον νόμο του Καρόλου)
- Πίεση (εξηγείται από τον νόμο του Μπόιλς)
Κατανόηση της επίδρασης της θερμοκρασίας στις καταστάσεις της ύλης
Σε ατμοσφαιρική πίεση, το νερό υπάρχει ως υγρό σε θερμοκρασίες μεταξύ 0°C και 100°C, ως υδρατμοί (αέριο) πέραν των 100°C και ως πάγος (στερεός) στους 0°C και κάτω. Τα εύρη θερμοκρασίας στα οποία υπάρχουν ουσίες σε μια συγκεκριμένη κατάσταση ποικίλλουν για κάθε ουσία.
Γνωρίζουμε ότι το νερό έχει τρεις καταστάσεις, αλλά τι γίνεται με άλλα στοιχεία και ενώσεις; Υπάρχουν ο σίδηρος, το οξυγόνο και το χλωριούχο ασβέστιο σε τρεις καταστάσεις;
Η εμφατική απάντηση είναι:«Όλη η ύλη υπάρχει σε διαφορετικές καταστάσεις, ανάλογα με τη θερμοκρασία και την πίεση».
Από τα παραπάνω, το οξυγόνο είναι αέριο στους> -182ᵒC, ενώ ο σίδηρος είναι αέριο στους 2860ᵒC. Όλη η ύλη μπορεί να υπάρχει στις τρεις καταστάσεις, αλλά οι θερμοκρασίες στις οποίες επιτυγχάνονται σε κάθε κατάσταση ποικίλλουν ευρέως.
Ο νόμος του Καρόλου διέπει τις καταστάσεις της ύλης
Ο νόμος του Καρόλου δηλώνει ότι ο όγκος μιας σταθερής ποσότητας αερίου είναι ευθέως ανάλογος με την απόλυτη θερμοκρασία του εάν η πίεση παραμένει σταθερή.
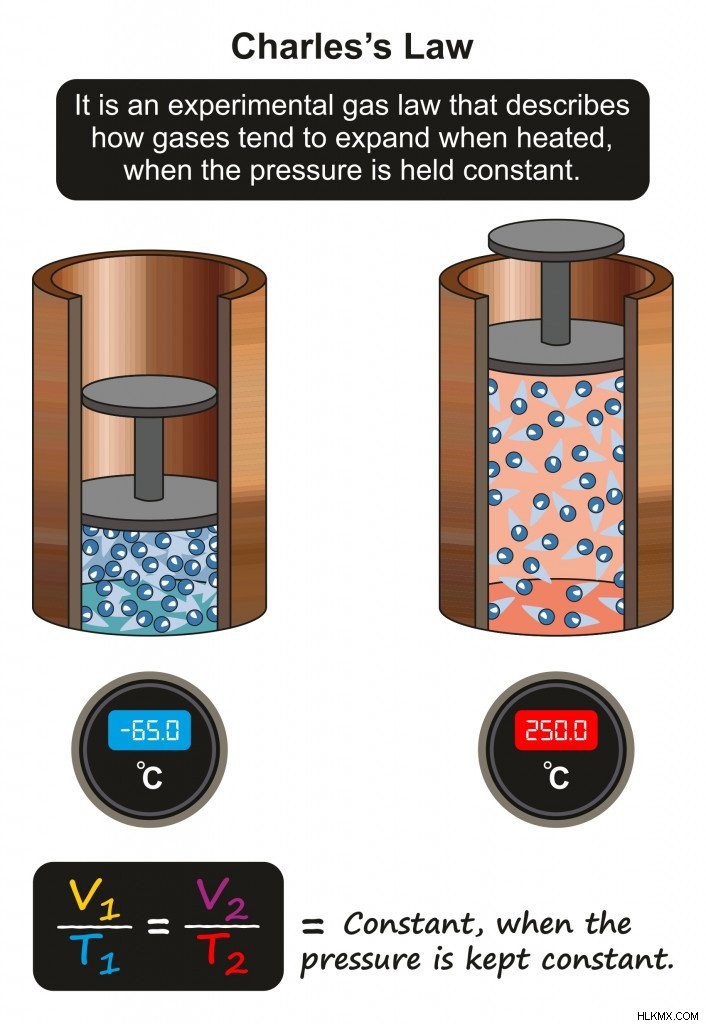
Ο νόμος του Καρόλου που υποθέτει τη σχέση μεταξύ της θερμοκρασίας και του όγκου (Photo Credit :udaix/Shutterstock)
Σε σταθερή πίεση, αν η θερμοκρασία ενός στερεού (δηλαδή του πάγου) αυξηθεί, ο όγκος του αντίστοιχα αυξάνεται. Με τον αυξημένο όγκο, τα μόρια μετακινούνται μακρύτερα, αυξάνοντας τη διαμοριακή απόσταση, μειώνοντας έτσι τις διαμοριακές δυνάμεις. Όταν συμβεί αυτό, ο στερεός πάγος υφίσταται αργά μια μετάβαση φάσης σε υγρό νερό.
Μια περαιτέρω αύξηση της θερμοκρασίας θα αυξήσει αναλογικά τον όγκο, κάνοντας τα μόρια να απομακρύνονται το ένα από το άλλο. Αυτό αυξάνει τη διαμοριακή απόσταση και μειώνει τη διαμοριακή δύναμη έλξης, προκαλώντας έτσι τη μετατόπιση από το νερό (υγρό) στον ατμό (αέριο).
Κατανόηση της επίδρασης της πίεσης στις Καταστάσεις της ύλης
Όπως αναφέρθηκε προηγουμένως, η πίεση είναι ένας άλλος κρίσιμος παράγοντας που καθορίζει την κατάσταση της ύλης. Αυτή η αρχή χρησιμοποιείται στην παρασκευή υγρού Ν2 και ξηρού πάγου (στερεό διοξείδιο του άνθρακα). Το αέριο άζωτο θα γίνει υγρό όταν αυξηθεί η πίεση στο αέριο.
Από την άλλη, μπορείτε να κάνετε το νερό να βράζει σε θερμοκρασία δωματίου μειώνοντας αρκετά την πίεση.
Άρα, η πίεση και η θερμοκρασία βρίσκονται σε αντίστροφη σχέση. Το υγρό N2 και ο ξηρός πάγος παράγονται εφαρμόζοντας πίεση στα αέρια N2 και CO2 για να αλλάξουν την κατάστασή τους από αέριο σε υγρό και αέριο σε στερεό, αντίστοιχα.

Liquid N2 (Photo Credit :Suslov Denis/Shutterstock)

Ξηρός πάγος (Φωτογραφία:Kollawat Somsri/Shutterstock)
Ο νόμος του Boyle διέπει τις καταστάσεις της ύλης
Όπως αναφέρθηκε προηγουμένως, υπάρχει μια αντίστροφη σχέση μεταξύ πίεσης και θερμοκρασίας, η οποία διέπεται από το νόμο του Boyle. Σύμφωνα με το νόμο, ο όγκος ενός αερίου αυξάνεται όσο μειώνεται η πίεση, σε σταθερή θερμοκρασία.
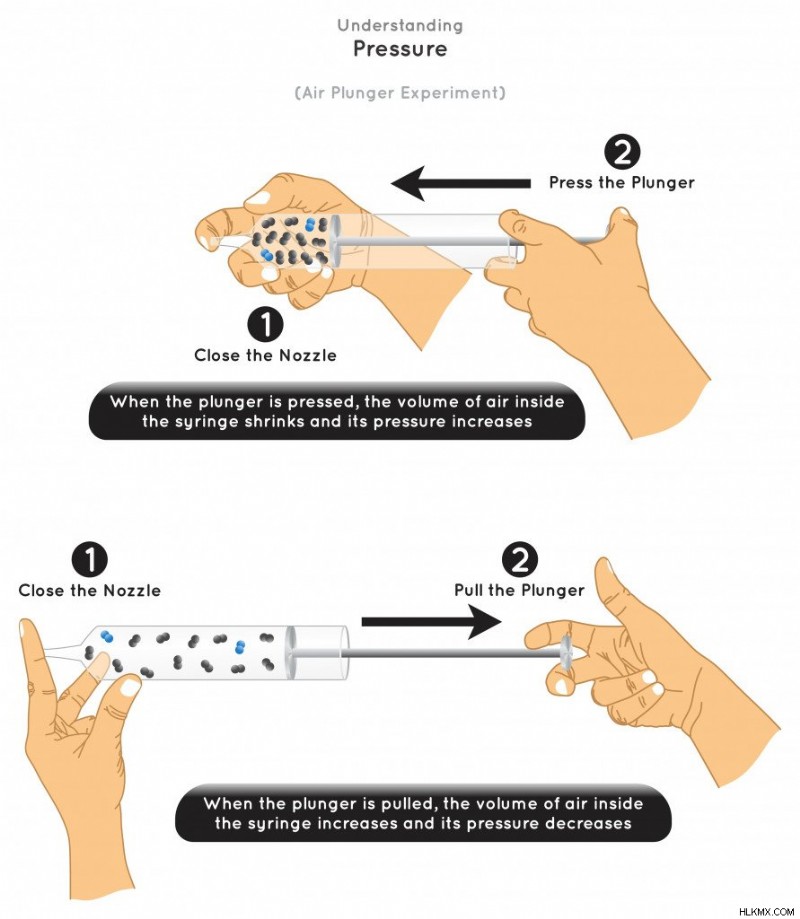
Ο νόμος του Boyle που υποθέτει τη σχέση μεταξύ πίεσης και όγκου (Photo Credit :udaix/Shutterstock)
Από την παραπάνω απεικόνιση, παρατηρούμε ότι η πίεση και ο όγκος ενός αερίου είναι αντιστρόφως ανάλογα.
Όταν η πίεση αυξάνεται, ο όγκος μειώνεται, φέρνοντας τα μόρια πιο κοντά μεταξύ τους. Αυτό αυξάνει τη διαμοριακή δύναμη έλξης και μειώνει τη διαμοριακή απόσταση. Αυτό θα προωθήσει τη μετάβαση από αέρια σε υγρή κατάσταση.
Μια περαιτέρω αύξηση της πίεσης μειώνει ακόμη περισσότερο τον όγκο, μεταφέροντας έτσι τα υγρά σε στερεά.
Πώς σχηματίζεται ο ξηρός πάγος;
Στην κατασκευή ξηρού πάγου, η πίεση στο αέριο CO2 μειώνεται από 1 ατμοσφαιρική (1 atm) σε 5,11. Σε αυτή την πίεση και σε σταθερή -56ⵒC, το αέριο CO2 γίνεται στερεό CO2 με μια πολύ παροδική υγρή κατάσταση.
Η συγκεκριμένη θερμοκρασία και πίεση στην οποία βρίσκονται σε ισορροπία τρεις καταστάσεις οποιασδήποτε ύλης ονομάζεται τριπλό σημείο της.
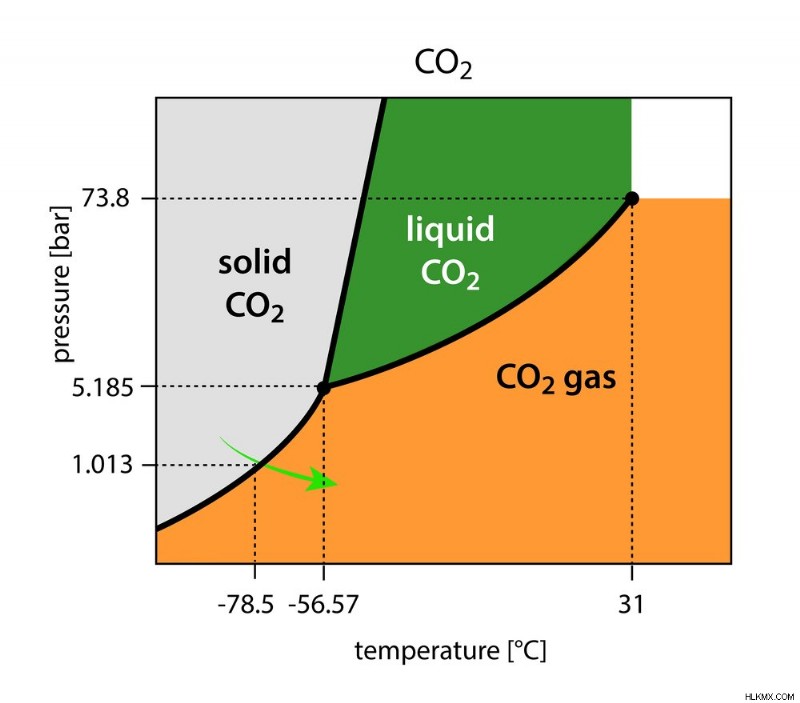
Τριπλό σημείο:Η θερμοκρασία και η πίεση στην οποία η στερεά, η υγρή και η αέρια φάση μιας καθαρής ουσίας μπορούν να συνυπάρχουν σε ισορροπία (Πιστωτική φωτογραφία :magnetix/Shutterstock)
Μια ελαφρά μείωση της θερμοκρασίας θα μετατρέψει σταδιακά το αέριο CO2 σε στερεό CO2.
Συμπεράσματα
Οι καταστάσεις της ύλης ανακυκλώνονται συνεχώς και η θερμοκρασία και η πίεση ελέγχουν τις μεταβάσεις φάσης. Η θερμοκρασία και η πίεση στην οποία συνυπάρχουν όλες οι καταστάσεις ονομάζεται τριπλό σημείο. Μια λεπτομερώς ενορχηστρωμένη διαδικασία μεταξύ θερμοκρασίας, όγκου και πίεσης καθορίζει την κατάσταση οποιουδήποτε θέματος.