Regelation of Ice in Physics and Chemistry
Η παλινδρόμηση είναι ένα φαινόμενο στη χημεία και τη φυσική που πιθανότατα έχετε δει, παρόλο που δεν γνωρίζατε το όνομά του. Μάθετε για το τι είναι η επαναρρύθμιση και δείτε παραδείγματα στην καθημερινή ζωή.
Ορισμός ρύθμισης
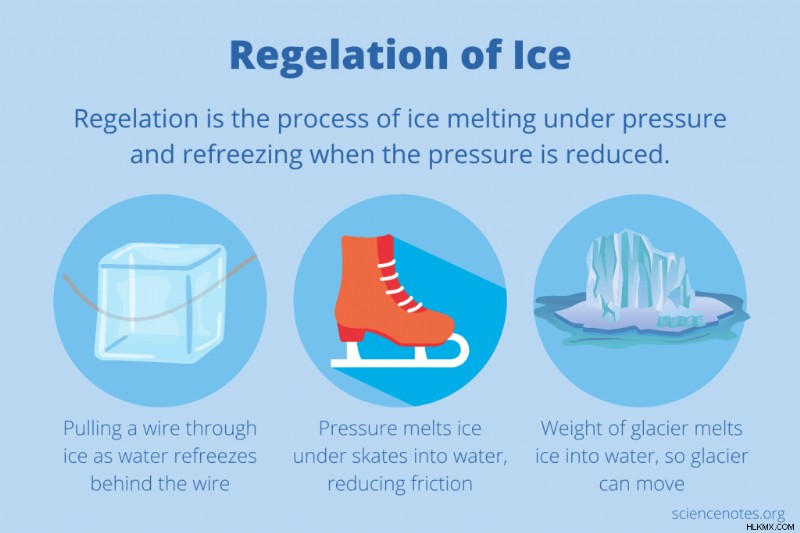
Η παλινδρόμηση είναι το φαινόμενο της τήξης του πάγου υπό πίεση και στη συνέχεια παγώματος ξανά μόλις εκτονωθεί η πίεση.
Επέκταση κατά την κατάψυξη
Η επαναρρύθμιση συμβαίνει μόνο για υλικά που διαστέλλονται κατά την κατάψυξη, έτσι ώστε το σημείο τήξης να μειώνεται καθώς αυξάνεται η εξωτερική πίεση. Για παράδειγμα, για 1 atm πίεσης που εφαρμόζεται, το σημείο τήξης του (νερού) πάγου πέφτει κατά 0,0072 °C. Αυτό σημαίνει ότι η παλινδρόμηση συμβαίνει σε άλλα υλικά, όπως το γάλλιο και το βισμούθιο. Αλλά, συνήθως, μια συζήτηση για την επαναρρύθμιση αφορά το νερό.
Παραδείγματα ρύθμισης
Τρία κοινά παραδείγματα παλινδρόμησης είναι η κίνηση του παγετώνα, το τράβηγμα ενός σύρματος μέσα από τον πάγο και το πατινάζ στον πάγο.
- Η επαναρρύθμιση εμφανίζεται στους παγετώνες. Η μάζα ενός παγετώνα ασκεί αρκετή πίεση για να μειώσει το σημείο τήξης του πάγου στη βάση του, λιώνοντας τον πάγο και αφήνοντας τον παγετώνα να γλιστρήσει πάνω από το υγρό. Κάτω από τις κατάλληλες συνθήκες, μπορεί να ρέει υγρό νερό από τη βάση ενός παγετώνα. Το νερό πίσω από τον παγετώνα ξαναπαγώνει.
- Ένα άλλο παράδειγμα παλινδρόμησης είναι η επίδειξη πάγου σε σύρμα. Περάστε ένα λεπτό σύρμα πάνω από ένα παγάκι και στερεώστε ένα μεγάλο βάρος στο σύρμα. Η πίεση που ασκεί το σύρμα στον πάγο τον λιώνει, επιτρέποντας στο σύρμα να περάσει μέσα από τον πάγο. Το νερό παγώνει ξανά πίσω από τη διαδρομή του σύρματος, ώστε να μπορείτε να τραβήξετε το σύρμα μέσα από τον πάγο, αφήνοντας το παγάκι ανέπαφο. Ενώ συμβαίνει επαναπήδηση, μέρος της τήξης προέρχεται από τη θέρμανση του σύρματος υπό τάση.
- Το πατινάζ στον πάγο λειτουργεί επειδή η πίεση του σκέιτερ πιέζει τη λεπίδα του πατινιού αρκετά προς τα κάτω για να λιώσει μέρος του πάγου σε νερό. Στη συνέχεια, το πατίνι γλιστρά πάνω από το νερό. Εάν η θερμοκρασία είναι πολύ κρύα, η πίεση είναι ανεπαρκής για να λιώσει ο πάγος και το πατινάζ δεν λειτουργεί. Πρόσθετοι παράγοντες παίζουν ρόλο στο πατινάζ στον πάγο, όχι απλώς η διαδικασία της παλινδρόμησης.
Λέγεται ότι οι χιονόμπαλες κολλάνε μεταξύ τους λόγω της παλινδρόμησης του χιονιού, αλλά αυτό δεν συμβαίνει. Ο σχηματισμός μιας χιονόμπαλας δεν απαιτεί αρκετή πίεση για να λιώσει ο πάγος. Το νερό που περιβάλλει τις νιφάδες χιονιού τις κολλάει μεταξύ τους. Το χιόνι δεν κολλάει όταν προσπαθείτε να φτιάξετε χιονόμπαλες σε εξαιρετικά κρύο καιρό.
Πώς λειτουργεί η ρύθμιση
Ο Michael Faraday περιέγραψε και ονόμασε πρώτος τη διαδικασία της παλινδρόμησης. Η διαδικασία οφείλεται στην ιδιαίτερη φύση του δεσμού υδρογόνου. Όταν ο πάγος συμπιέζεται, η απόσταση O:H (μη δεσμός) μειώνεται ενώ ο ομοιοπολικός δεσμός H-O επιμηκύνεται και εξασθενεί προς το O:H. Η πτώση του σημείου τήξης εμφανίζεται καθώς ο δεσμός H-O χάνει ενέργεια. Το σημείο τήξης είναι ανάλογο με τη συνεκτική ενέργεια του ομοιοπολικού δεσμού. Ουσιαστικά, το όριο φάσης μεταξύ της υγρής και στερεάς φάσης του νερού αλλάζει. Η απελευθέρωση της πίεσης επιτρέπει στον δεσμό O:H-O να επιστρέψει στην αρχική του κατάσταση, παγώνοντας ξανά το νερό σε πάγο. Η διαδικασία είναι ένα παράδειγμα μνήμης δεσμών υδρογόνου.
Ένα σχετικό αποτέλεσμα είναι ο πιεζοηλεκτρισμός. Ο πιεζοηλεκτρισμός είναι η συσσώρευση ηλεκτρικού φορτίου σε στερεά υλικά όταν ασκείται μηχανική καταπόνηση σε αυτά.
Αναφορές
- Drake, L. D.; Shreve, R. L. (1973). «Τήξη υπό πίεση και επαναπήδηση πάγου με στρογγυλά σύρματα». Πρακτικά της Βασιλικής Εταιρείας Α:Μαθηματικές, Φυσικές και Μηχανικές Επιστήμες . 332 (1588):51. doi:10.1098/rspa.1973.0013
- Sun, Chang Qing (2014). Χαλάρωση του χημικού δεσμού . Πηδών. ISBN 978-981-4585-20-0.
- Sun, Chang Qing; et al. (2012). «Κρυμμένη δύναμη που αντιτίθεται στη συμπίεση του πάγου». Chem Science 3 :1455-1460. doi:10.1039/c2sc20066j
- Zhang, Xi; et al. (Οκτώβριος 2014). «Ένα κοινό υπερολισθηρό δέρμα που καλύπτει τόσο νερό όσο και πάγο». Φυσικοχημεία Χημική Φυσική. 16 (42):22987–22994. doi:10.1039/C4CP02516D