Ορισμός Ατομικού Πυρήνα και Γεγονότα
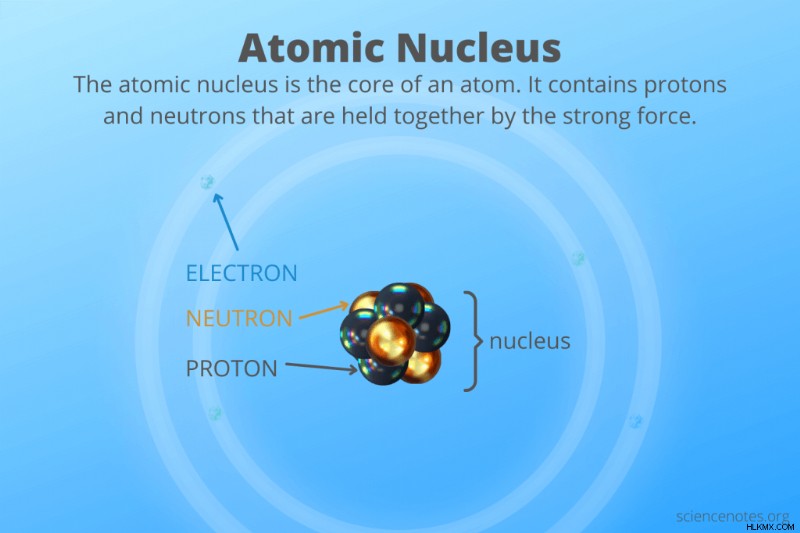
Οατομικός πυρήνας είναι ο μικροσκοπικός, πυκνός πυρήνας ενός ατόμου που περιέχει πρωτόνια και νετρόνια που συγκρατούνται μεταξύ τους από την ισχυρή δύναμη. Συλλογικά, τα πρωτόνια και τα νετρόνια στον πυρήνα ονομάζονται νουκλεόνια. Ο αριθμός των πρωτονίων στον ατομικό πυρήνα προσδιορίζει το στοιχείο ενός ατόμου. Γνωρίζοντας το στοιχείο, ο αριθμός των νετρονίων στον πυρήνα προσδιορίζει το ισότοπό του.
- Ο ατομικός πυρήνας αποτελείται από πρωτόνια και νετρόνια.
- Ο πυρήνας έχει θετικό ηλεκτρικό φορτίο.
- Η πυρηνική σύνθεση καθορίζει το στοιχείο ενός ατόμου (αριθμός πρωτονίων) και το ισότοπο (αριθμός νετρονίων).
- Ο πυρήνας είναι πολύ μικρός και πυκνός. Αντιπροσωπεύει σχεδόν όλη την ατομική μάζα, αλλά πολύ λίγο από τον όγκο της.
Προέλευση λέξης
Η λέξη πυρήνας προέρχεται από τη λατινική λέξη nucleus , που σημαίνει «πυρήνας» ή «καρύδι». Ο Michael Faraday αναφέρθηκε στο κέντρο του ατόμου ως πυρήνας το 1844 και ο Rutherford χρησιμοποίησε τον όρο το 1912. Ωστόσο, άλλοι επιστήμονες δεν τον υιοθέτησαν αμέσως και αναφέρθηκαν στον ατομικό πυρήνα ως πυρήνα για αρκετά χρόνια.
Ιστορικό
Η ανακάλυψη του ατομικού πυρήνα από τον Έρνεστ Ράδερφορντ το 1911 εντοπίζει τις ρίζες της στο πείραμα με φύλλο χρυσού Geiger-Marsden το 1909. Το πείραμα με φύλλο χρυσού περιελάμβανε εκτόξευση σωματιδίων άλφα (πυρήνες ηλίου) σε ένα λεπτό φύλλο χρυσού. Εάν τα σωματίδια άλφα περνούσαν εύκολα μέσα από τον χρυσό, θα υποστήριζε το «μοντέλο πουτίγκας δαμάσκηνου» του ατόμου του J. J. Thomson, με ένα άτομο που αποτελείται από αναμειγνύοντας θετικό και αρνητικό φορτίο. Ωστόσο, πολλά από τα σωματίδια άλφα αναπήδησαν μακριά από το φύλλο, που σημαίνει ότι τα άτομα αποτελούνται από ξεχωριστές περιοχές θετικού και αρνητικού φορτίου.
Η ανακάλυψη του νετρονίου το 1932 οδήγησε σε μια καλύτερη κατανόηση της φύσης του ατομικού πυρήνα. Ο Ντμίτρι Ιβανένκο και ο Βέρνερ Χάιζενμπεργκ πρότειναν ένα μοντέλο του ατόμου με έναν θετικά φορτισμένο πυρήνα που περιβάλλεται από ένα νέφος αρνητικά φορτισμένων ηλεκτρονίων.
Τι Περιέχει ο Ατομικός Πυρήνας;
Ο ατομικός πυρήνας αποτελείται από πρωτόνια και νετρόνια. Τα πρωτόνια και τα νετρόνια αποτελούνται από υποατομικά σωματίδια που ονομάζονται κουάρκ. Τα κουάρκ ανταλλάσσουν έναν άλλο τύπο υποατομικών σωματιδίων (γκλουόνια). Αυτή η ανταλλαγή είναι η ισχυρή δύναμη που ενώνει τα σωματίδια μεταξύ τους μέσα στον πυρήνα. Η ισχυρή δύναμη δρα σε μικρή απόσταση, αλλά είναι πιο ισχυρή από την ηλεκτροστατική απώθηση μεταξύ θετικά φορτισμένων πρωτονίων.
Ενώ συνήθως θεωρούμε τα πρωτόνια και τα νετρόνια ως σωματίδια, έχουν επίσης ιδιότητες κυμάτων. Επειδή τα πρωτόνια και τα νετρόνια έχουν διαφορετικές κβαντικές καταστάσεις, μπορούν να μοιράζονται την ίδια κυματική λειτουργία του διαστήματος. Στην πραγματικότητα, δύο πρωτόνια, δύο νετρόνια ή ένα πρωτόνιο και ένα νετρόνιο σχηματίζουν ένα νουκλεόνιο, με τα δύο σωματίδια να μοιράζονται τον ίδιο χώρο.
Αν και δεν παρατηρούνται στη φύση, τα πειράματα φυσικής υψηλής ενέργειας αναφέρουν μερικές φορές ένα τρίτο βαρυόνιο, που ονομάζεται υπερόν. Ένα υπερόνιο είναι ένα υποατομικό σωματίδιο που μοιάζει πολύ με ένα πρωτόνιο ή ένα νετρόνιο, εκτός από το ότι περιέχει ένα ή περισσότερα περίεργα κουάρκ.
Συνήθως, ο πυρήνας δεν περιέχει ηλεκτρόνια επειδή διασκορπίζονται μακριά από τον ατομικό πυρήνα. Ωστόσο, η κυματική συνάρτηση που περιγράφει την πιθανότητα εύρεσης ηλεκτρονίου σε οποιαδήποτε συγκεκριμένη περιοχή περνάει από τον πυρήνα.
Πόσο μεγάλος είναι ο ατομικός πυρήνας;
Ο ατομικός πυρήνας είναι εξαιρετικά μικροσκοπικός, αλλά πολύ πυκνός. Αντιπροσωπεύει λιγότερο από το ένα δέκα τρισεκατομμύριο του όγκου ενός ατόμου, αλλά περίπου το 99,9994% της μάζας ενός ατόμου. Για να το θέσουμε διαφορετικά, ένα άτομο στο μέγεθος ενός γηπέδου ποδοσφαίρου έχει πυρήνα στην πλευρά ενός μπιζελιού.
Το μέσο μέγεθος ενός ατομικού πυρήνα κυμαίνεται μεταξύ 1,8 × 10 m (υδρογόνο) και 11,7 × 10 m (ουράνιο). Αντίθετα, το μέσο μέγεθος ενός ατόμου κυμαίνεται μεταξύ 52,92 x 10 m (υδρογόνο) και 156 x 10 m (ουράνιο). Αυτή είναι μια διαφορά περίπου 60.000 για το υδρογόνο και 27.000 για το ουράνιο.
Ποιο είναι το σχήμα του ατομικού πυρήνα;
Τυπικά, το σχήμα του ατομικού πυρήνα είναι στρογγυλό ή ελλειψοειδές. Ωστόσο, εμφανίζονται και άλλα σχήματα. Εδώ είναι τα σχήματα πυρήνων που έχουν παρατηρηθεί μέχρι σήμερα:
- Σφαιρικό
- Παρατμορφωμένος προπύργιος (σαν μπάλα ράγκμπι)
- Παραμμορφωμένη πλάκα (σαν δίσκος)
- Τριαξονικό (όπως ένας συνδυασμός μπάλας ράγκμπι και δίσκου)
- Σχήμα αχλαδιού
- Σχήμα αλόου (ένας μικρός πυρήνας που περιβάλλεται από ένα φωτοστέφανο περίσσειας πρωτονίων ή νετρονίων)
Μοντέλα
Ένα διάγραμμα ατόμου συνήθως απεικονίζει τον πυρήνα ως ένα σύμπλεγμα πρωτονίων και νετρονίων ίσου μεγέθους με ηλεκτρόνια σε τροχιά. Φυσικά, πρόκειται για υπεραπλούστευση. Υπάρχουν πολλά μοντέλα του ατομικού πυρήνα:
- Μοντέλο συμπλέγματος :Το μοντέλο συστάδας περιλαμβάνει αυτό που βλέπετε στα διαγράμματα, με πρωτόνια και νετρόνια ομαδοποιημένα. Τα σύγχρονα μοντέλα συστάδων είναι πιο περίπλοκα, με τα συμπλέγματα δύο και τριών σωμάτων να σχηματίζουν πιο πολύπλοκες πυρηνικές δομές.
- Μοντέλο σταγόνας υγρού :Σε αυτό το μοντέλο, ο πυρήνας λειτουργεί ως περιστρεφόμενη σταγόνα υγρού. Αυτό το μοντέλο εξηγεί το μέγεθος, τη σύνθεση και την ενέργεια δέσμευσης των πυρήνων, αλλά δεν εξηγεί τη σταθερότητα των «μαγικών αριθμών» πρωτονίων και νετρονίων.
- Μοντέλο Shell :Αυτό το μοντέλο βλέπει τη δομή των νουκλεονίων σαν τη δομή των ηλεκτρονίων, όπου τα νουκλεόνια καταλαμβάνουν τροχιακά. Η τοποθέτηση πρωτονίων και νετρονίων σε τροχιακά προβλέπει με επιτυχία τον μαγικό αριθμό επειδή τα μοντέλα επιτρέπουν σταθερές διαμορφώσεις. Τα μοντέλα κελύφους καταρρέουν όταν συζητείται η πυρηνική συμπεριφορά εκτός των κλειστών πυρηνικών κελυφών.
Αναφορές
- Cook, N.D. (2010). Μοντέλα του Ατομικού Πυρήνα (2η έκδ.). Πηδών. ISBN 978-3-642-14736-4.
- Heyde, Kris (1999). Βασικές ιδέες και έννοιες στην πυρηνική φυσική:Μια εισαγωγική προσέγγιση (2η έκδ.). Philadelphia:Institute of Physics Publishers.
- Iwanenko, D.D. (1932). «Η υπόθεση των νετρονίων». Φύση . 129 (3265):798. doi:10.1038/129798d0
- Krane, K.S. (1987). Εισαγωγική Πυρηνική Φυσική . Wiley-VCH. ISBN 978-0-471-80553-3.
- Miller, Α. Ι. (1995). Πρώιμη Κβαντική Ηλεκτροδυναμική:Ένα Βιβλίο Πηγών . Cambridge:Cambridge University Press. ISBN 0521568919.
- Sobczyk, J. E.; Acharya, Β.; Bacca, S.; Hagen, G. (2021). "Ab Initio Υπολογισμός της συνάρτησης διαμήκους απόκρισης σε Ca“. Φυσ. Σεβ. Lett . 127.




