Διαφορά μεταξύ βουτανίου και βουτενίου
Κύρια διαφορά – Βουτάνιο εναντίον Βουτενίου
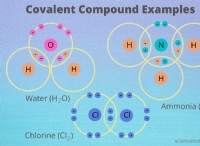
Το βουτάνιο και το βουτένιο είναι αέριες ενώσεις που αποτελούνται από άτομα C και H. Ονομάζονται υδρογονάνθρακες λόγω της παρουσίας μόνο ατόμων C και H. Και τα δύο αυτά μόρια αποτελούνται από 4 άτομα άνθρακα ανά μόριο. Η κύρια πηγή βουτανίου και βουτενίου είναι το αργό πετρέλαιο. Επομένως, αυτά τα αέρια μπορούν να ληφθούν ως υποπροϊόν των διεργασιών διύλισης πετρελαίου. Αλλά υπάρχουν ως δευτερεύοντες υποκαταστάτες στο αργό πετρέλαιο. Δεδομένου ότι αυτά τα αέρια είναι εύφλεκτα, μπορούν να χρησιμοποιηθούν ως καύσιμο. Η πλήρης καύση βουτανίου και βουτενίου παράγει διοξείδιο του άνθρακα και υδρατμούς μαζί με τη θερμότητα. Αλλά η ατελής καύση θα παράγει μονοξείδιο του άνθρακα αντί για διοξείδιο του άνθρακα και λιγότερη ποσότητα θερμότητας από αυτή της πλήρους καύσης. Η κύρια διαφορά μεταξύ βουτανίου και βουτενίου είναι ότι δεν υπάρχουν διπλοί δεσμοί στα μόρια βουτανίου ενώ τα μόρια βουτενίου έχουν έναν διπλό δεσμό.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το βουτάνιο
– Ορισμός, ιδιότητες και εφαρμογές
2. Τι είναι το Butene
– Ορισμός, ιδιότητες και εφαρμογές
3. Ποιες είναι οι ομοιότητες μεταξύ βουτανίου και βουτενίου
– Περίληψη κοινών χαρακτηριστικών
4. Ποια είναι η διαφορά μεταξύ βουτανίου και βουτενίου
– Σύγκριση βασικών διαφορών
Βασικοί όροι:βουτάνιο, βουτένιο, καύση, αργό πετρέλαιο, υδρογονάνθρακες, πετρέλαιο 
Τι είναι το βουτάνιο
Το βουτάνιο είναι ένας υδρογονάνθρακας που έχει τον χημικό τύπο C4 H10 . Είναι ένα άχρωμο αέριο σε θερμοκρασία και πίεση δωματίου. Η μοριακή μάζα αυτής της ένωσης είναι περίπου 58,12 g/mol. Έχει μυρωδιά σαν βενζίνη. Ανήκει στην ομάδα των αλκανίων αφού δεν έχει διπλούς δεσμούς στη δομή του. Το βουτάνιο είναι μια μη πολική ένωση. Επομένως, δεν διαλύεται σε πολικούς διαλύτες ή νερό. Τα μόρια βουτανίου μπορεί να υπάρχουν σε δύο διαφορετικά δομικά ισομερή. Είναι n-βουτάνιο και ισοβουτάνιο. Το n-βουτάνιο είναι η γραμμική, ευθεία αλυσίδα του βουτανίου, ενώ το ισοβουτάνιο είναι μια διακλαδισμένη δομή.
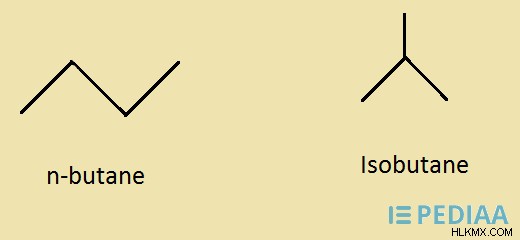
Εικόνα 1:Δομικά ισομερή βουτανίου
Το βουτάνιο είναι πολύ εύφλεκτο. Υγροποιείται εύκολα. Δεδομένου ότι το σημείο βρασμού του βουτανίου είναι περίπου 1 C (ή λιγότερο), αυτό το υγρό βουτανίου εξατμίζεται γρήγορα σε θερμοκρασία δωματίου. Όταν υπάρχει αρκετό οξυγόνο στο περιβάλλον, το βουτάνιο μπορεί να υποστεί πλήρη καύση, σχηματίζοντας διοξείδιο του άνθρακα και υδρατμούς μαζί με θερμική ενέργεια. Αλλά εάν το οξυγόνο δεν είναι αρκετό, τότε το βουτάνιο θα υποστεί ατελή καύση, παράγοντας μονοξείδιο του άνθρακα και σκόνη του άνθρακα.
Μπορεί να προστεθεί βουτάνιο στη βενζίνη για να σταθεροποιηθεί η εξάτμιση της βενζίνης. Αυτή είναι μια από τις κύριες χρήσεις του βουτανίου. Μπορεί επίσης να χρησιμοποιηθεί ως διαλύτης για εκχυλίσεις, καθώς το βουτάνιο είναι εξαιρετικά μη πολικό και λιγότερο αντιδραστικό. Επιπλέον, το βουτάνιο χρησιμοποιείται ως καύσιμο σε εφαρμογές μικρής κλίμακας.
Τι είναι το Butene
Το βουτένιο είναι ένας υδρογονάνθρακας που έχει τον χημικό τύπο C4 H8 . Είναι ένα άχρωμο αέριο σε θερμοκρασία και πίεση δωματίου. Έχει μια ελαφρώς αρωματική μυρωδιά. Το βουτένιο είναι ένα αλκένιο. Η κύρια πηγή βουτενίου είναι το αργό πετρέλαιο. Το βουτένιο υπάρχει στο αργό πετρέλαιο ως δευτερεύον συστατικό. Το βουτένιο μπορεί να βρεθεί σε πολλά ισομερή. Ωστόσο, το βουτένιο έχει έναν διπλό δεσμό μεταξύ δύο από τα άτομα άνθρακα. Η μοριακή μάζα του βουτενίου είναι περίπου 56,11 g/mol.

Εικόνα 2:Cis-trans ισομερισμός του βουτενίου
Η ισομέρεια του βουτενίου εμφανίζεται είτε ως δομική ισομέρεια είτε ως στερεοϊσομέρεια. Η θέση του διπλού δεσμού καθορίζει τη δομική ισομέρεια. Το 1-βουτένιο έχει τον διπλό δεσμό στο τέλος της ανθρακικής αλυσίδας ενώ το 2-βουτένιο έχει τον διπλό δεσμό στη μέση της ανθρακικής αλυσίδας. Επιπλέον, η διακλαδισμένη δομή ισοβουτυλένιο είναι ένα άλλο δομικό ισομερές του γραμμικού μορίου βουτενίου. Η στερεοϊσομέρεια εμφανίζεται σύμφωνα με τις διαφορές στη θέση των αλκυλομάδων στα αλλυλικά άτομα άνθρακα. Αυτό ονομάζεται γεωμετρική ισομέρεια.
Το βουτένιο παράγεται στη διύλιση πετρελαίου. Η παραγωγή βουτενίου γίνεται μέσω αντίδρασης πυρόλυσης. Αυτή είναι η διάσπαση των υδρογονανθράκων μακράς αλυσίδας σε μικρά μόρια υδρογονανθράκων. Το βουτένιο είναι εύφλεκτο αέριο και μπορεί να χρησιμοποιηθεί ως καύσιμο. Το βουτένιο είναι ένα σημαντικό μονομερές στην παραγωγή πολυμερών. Ο διπλός δεσμός που υπάρχει στο βουτένιο του επιτρέπει να υποστεί πολυμερισμό ο οποίος τελικά θα παράγει ένα μόριο πολυμερούς.
Ομοιότητες μεταξύ βουτανίου και βουτενίου
- Το βουτάνιο και το βουτένιο είναι υδρογονάνθρακες.
- Πρόκειται για αέρια σε θερμοκρασία και πίεση δωματίου.
- Και τα δύο είναι άχρωμα αέρια.
- Το βουτάνιο και το βουτένιο μπορούν να ληφθούν από διεργασίες διύλισης πετρελαίου.
- Και τα δύο είναι πολύ εύφλεκτα.
- Και οι δύο τύποι δείχνουν ισομερισμό.
Διαφορά μεταξύ Βουτάνιου και Βουτενίου
Ορισμός
Βουτάνιο: Το βουτάνιο είναι ένας υδρογονάνθρακας που έχει τον χημικό τύπο C4 H10 .
Βουτένιο: Το βουτένιο είναι ένας υδρογονάνθρακας που έχει τον χημικό τύπο C4 H8 .
Χημικός δεσμός
Βουτάνιο: Το βουτάνιο έχει μόνο απλούς δεσμούς.
Βουτένιο: Το βουτένιο έχει διπλό δεσμό καθώς και απλούς δεσμούς.
Ταξινόμηση
Βουτάνιο: Το βουτάνιο είναι ένα αλκάνιο.
Βουτένιο: Το βουτένιο είναι ένα αλκένιο.
Ισομέρεια Cis-trans
Βουτάνιο: Το βουτάνιο δεν εμφανίζει ισομερισμό cis-trans.
Βουτένιο: Το βουτένιο εμφανίζει cis-trans ισομέρεια.
Μοριακή μάζα
Βουτάνιο: Η μοριακή μάζα του βουτανίου είναι 58,12 g/mol.
Βουτένιο: Η μοριακή μάζα του βουτενίου είναι περίπου 56,11 g/mol.
Συμπέρασμα
Αέρια βουτάνιο και βουτένιο μπορούν να χρησιμοποιηθούν ως καύσιμο. Αυτά τα αέρια παράγουν θερμότητα όταν καίγονται. Επιπλέον, το βουτάνιο χρησιμοποιείται ως διαλύτης για εκχυλίσεις λόγω των μη πολικών ιδιοτήτων του. Το βουτένιο είναι ένα μονομερές για την παραγωγή διαφορετικών τύπων πολυμερών. Ο διπλός δεσμός που υπάρχει στο βουτένιο του επιτρέπει να ενεργεί ως μονομερές. Η κύρια διαφορά μεταξύ βουτανίου και βουτενίου είναι ότι δεν υπάρχουν διπλοί δεσμοί στα μόρια βουτανίου ενώ τα μόρια βουτενίου έχουν έναν διπλό δεσμό.