Διαφορά μεταξύ νικελίου και αργύρου
Κύρια διαφορά – Νικέλιο εναντίον Ασημί
Το ασήμι και το νικέλιο είναι δύο μεταλλικά στοιχεία που βρίσκονται στο μπλοκ d του περιοδικού πίνακα στοιχείων. Το νικέλιο και ο άργυρος είναι πολύ ανθεκτικά στη διάβρωση. Ως εκ τούτου, έχουν μια μεγάλη ποικιλία εφαρμογών. Το ασήμι μέταλλο μπορεί να βρεθεί στην καθαρή του μορφή φυσικά. Μπορεί επίσης να βρεθεί ως κράμα μετάλλων με χρυσό ή άλλα μέταλλα και ως συστατικό σε ορισμένα ορυκτά. Πολύ ίχνη νικελίου μπορούν επίσης να βρεθούν στην καθαρή του μορφή. Αλλά η πλειονότητα των πηγών νικελίου στη γη δεν είναι προσβάσιμη αφού βρίσκονται στον πυρήνα της γης. Είναι συχνά δύσκολο να εντοπιστεί η διαφορά μεταξύ νικελίου και ασημιού λόγω της λαμπερής εμφάνισής τους. Αν και αυτά τα μέταλλα μοιάζουν με την εμφάνισή τους, υπάρχουν αρκετές διαφορές μεταξύ των δύο στοιχείων. Η κύρια διαφορά μεταξύ του νικελίου και του αργύρου είναι ότι το σημείο τήξης του νικελίου είναι πολύ υψηλό σε σύγκριση με το σημείο τήξης του αργύρου.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το νικέλιο
– Ορισμός, Ιδιότητες, Αντιδράσεις και Χρήσεις
2. Τι είναι το Silver
– Ορισμός, Ιδιότητες, Αντιδράσεις και Χρήσεις
3. Ποια είναι η διαφορά μεταξύ Νικελίου και Ασημιού
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Χρυσός, Κράμα μετάλλων, Ορυκτά, Νικέλιο (Ni), Ασήμι (Ag) 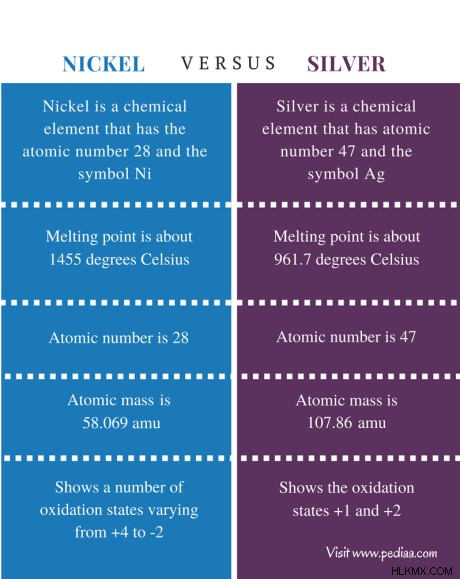
Τι είναι το νικέλιο
Το νικέλιο είναι ένα χημικό στοιχείο που έχει ατομικό αριθμό 28 και σύμβολο Ni . Είναι ένα φυσικό μεταλλικό στοιχείο. Το νικέλιο έχει πολύ λαμπερή εμφάνιση. Είναι ένα στοιχείο d block στον περιοδικό πίνακα και είναι ένα μέταλλο μετάπτωσης. Η διαμόρφωση ηλεκτρονίων του Νικελίου είναι [Ar]3d4s. Σε θερμοκρασία δωματίου και πίεση, είναι σε στερεή κατάσταση. Η ατομική μάζα του Νικελίου είναι περίπου 58.069 amu.
Το σημείο τήξης του νικελίου είναι ένα από τα κύρια χαρακτηριστικά του. Είναι πολύ υψηλής τιμής και έχει μετρηθεί ως 1455C. Το νικέλιο είναι επίσης πολύ ανθεκτικό στη διάβρωση και την οξείδωση. Ένα άλλο από τα σημαντικά χαρακτηριστικά του είναι η υψηλή ολκιμότητα. Αυτό σημαίνει ότι το νικέλιο μπορεί να έλκεται σε δομές που μοιάζουν με σύρμα.
Το νικέλιο μπορεί να σχηματίσει έναν αριθμό διαφορετικών ενώσεων αφού εμφανίζει πολλές καταστάσεις οξείδωσης, συμπεριλαμβανομένων των 0, +1, +2, +3, +4 και -1, -2 . Η πιο κοινή κατάσταση οξείδωσης είναι +2. Τα υδατικά διαλύματα Ni είναι πράσινου χρώματος. Επιπλέον, το Ni σχηματίζει μια σειρά από πολύχρωμα σύμπλοκα αμίνης.

Εικόνα 1:Πολύχρωμα σύμπλοκα νικελίου
Το νικέλιο είναι ένα από τα λίγα σιδηρομαγνητικά στοιχεία. Σε θερμοκρασία δωματίου, έλκεται πολύ από τους μαγνήτες. Υπάρχουν πολλά ισότοπα στο νικέλιο. Το Ni είναι το πιο άφθονο ισότοπο μεταξύ άλλων ισοτόπων. Η αφθονία του είναι περίπου 68%. Είναι το πιο σταθερό ισότοπο του Νικελίου. Το Ni είναι επίσης σταθερό αλλά είναι λιγότερο άφθονο (περίπου 26%).
Τι είναι το Silver
Το ασήμι είναι ένα χημικό στοιχείο που έχει ατομικό αριθμό 47 και το σύμβολο Ag . Αν και το όνομά του είναι ασήμι, του δίνεται το σύμβολο Ag επειδή η λατινική λέξη Argentum σημαίνει ασήμι. Το ασήμι μπορεί να βρεθεί ως καθαρό μέταλλο στη φύση. Μπορεί να βρεθεί ως κράμα μετάλλων με χρυσό ή άλλα μεταλλικά στοιχεία και ως συστατικό σε ορισμένες ορυκτές ενώσεις. Η ατομική μάζα του αργύρου είναι 107,86 amu. Η διαμόρφωση ηλεκτρονίων δίνεται ως [Kr]4d5s.
Σε θερμοκρασία και πίεση δωματίου, το ασήμι είναι ένα συμπαγές μέταλλο. Έχει λαμπερή λάμψη. Το ασήμι ανήκει στο μπλοκ d του περιοδικού πίνακα στοιχείων. Το σημείο τήξης του αργύρου είναι περίπου 961,7 C. Οι πιο κοινές καταστάσεις οξείδωσης του αργύρου είναι +1 και +2. Υπάρχουν δύο κύρια ισότοπα του αργύρου. είναι ο Αγ και ο Αγ. Και τα δύο ισότοπα είναι κάπως εξίσου άφθονα στη φύση. Ωστόσο, το Ag είναι ελαφρώς πιο άφθονο από το ισότοπο Ag. Υπάρχουν μερικά συνθετικά ισότοπα αργύρου που είναι ραδιενεργά.
Μεταξύ των χημικών αντιδράσεων του αργύρου, ο σχηματισμός αλογονιδίων μετάλλων είναι μια κοινή αντίδραση. Ο χλωριούχος άργυρος, ο βρωμιούχος άργυρος και ο ιωδιούχος άργυρος είναι ιζήματα. Ως εκ τούτου, μερικές φορές μπορεί να χρησιμοποιηθεί για να διαπιστωθεί η παρουσία ιόντων αργύρου σε ένα διάλυμα. Το ασήμι σχηματίζει επίσης ενώσεις συντονισμού.

Εικόνα 2:Το ασήμι χρησιμοποιείται στην παραγωγή νομισμάτων
Το ασήμι χρησιμοποιείται συνήθως στην παραγωγή νομισμάτων και κοσμημάτων. Υπάρχουν και φαρμακευτικές εφαρμογές του αργύρου. Εδώ, το ασήμι χρησιμοποιείται για επιδέσμους τραυμάτων, μερικές φορές χρησιμοποιείται για τη θεραπεία εξωτερικών λοιμώξεων και χρησιμοποιείται ως συστατικό σε αλοιφές που χρησιμοποιούνται για τη θεραπεία τραυμάτων που προκαλούνται από εγκαύματα.
Διαφορά μεταξύ Νικελίου και Ασημιού
Ορισμός
Νίκελο: Το νικέλιο είναι ένα χημικό στοιχείο που έχει τον ατομικό αριθμό 28 και το σύμβολο Ni.
Ασημί: Ο άργυρος είναι ένα χημικό στοιχείο που έχει ατομικό αριθμό 47 και το σύμβολο Ag.
Σημείο τήξης
Νίκελο: Το σημείο τήξης του νικελίου είναι περίπου 1455 C.
Ασημί: Το σημείο τήξης του αργύρου είναι περίπου 961,7 C.
Ατομικός αριθμός
Νίκελο: Ο ατομικός αριθμός του νικελίου είναι 28.
Ασημί: Ο ατομικός αριθμός του αργύρου είναι 47.
Ατομική μάζα
Νίκελο: Η ατομική μάζα του νικελίου είναι 58,069 amu.
Ασημί: Η ατομική μάζα του αργύρου είναι 107,86 amu.
Καταστάσεις οξείδωσης
Νίκελο: Το νικέλιο εμφανίζει έναν αριθμό καταστάσεων οξείδωσης που ποικίλλουν από +4 έως -2.
Ασημί: Το ασήμι δείχνει τις καταστάσεις οξείδωσης +1 και +2.
Συμπέρασμα
Το νικέλιο και το ασήμι είναι πολύ χρήσιμα μέταλλα για την παραγωγή διαφορετικού εξοπλισμού και άλλων υλικών. Αλλά οι εφαρμογές τους είναι διαφορετικές μεταξύ τους λόγω των διαφόρων ιδιοτήτων αυτών των μετάλλων. Για παράδειγμα, το νικέλιο μπορεί να χρησιμοποιηθεί για την παραγωγή υλικών που χρησιμοποιούνται σε συνθήκες υψηλής θερμοκρασίας λόγω της διαφοράς μεταξύ των σημείων τήξης αυτών των στοιχείων, η οποία είναι επίσης η κύρια διαφορά μεταξύ νικελίου και αργύρου.