Διαφορά μεταξύ συντονισμού και μεσομερικού φαινομένου
Κύρια διαφορά – Συντονισμός έναντι μεσομερικού φαινομένου
Ο συντονισμός και τα μεσομερικά αποτελέσματα στα μόρια καθορίζουν την ακριβή χημική δομή του μορίου. Ο συντονισμός είναι το φαινόμενο που περιγράφει την πολικότητα ενός μορίου που προκαλείται από την αλληλεπίδραση μεταξύ μονών ζευγών ηλεκτρονίων και ζευγών ηλεκτρονίων δεσμού. Μεσομερική επίδραση είναι η επίδραση υποκαταστατών ή λειτουργικών ομάδων σε χημικές ενώσεις. Η κύρια διαφορά μεταξύ συντονισμού και μεσομερούς φαινομένου είναι ότι ο συντονισμός εμφανίζεται λόγω της αλληλεπίδρασης μεταξύ μοναχικών ζευγών ηλεκτρονίων και ζευγών ηλεκτρονίων δεσμού, ενώ το μεσομερές φαινόμενο εμφανίζεται λόγω της παρουσίας υποκαταστατών ομάδων ή λειτουργικών ομάδων.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το Resonance
– Ορισμός, περιγραφή με παραδείγματα
2. Τι είναι το Mesomeric Effect
– Ορισμός, περιγραφή με παραδείγματα
3. Ποια είναι η διαφορά μεταξύ συντονισμού και μεσομερικού φαινομένου
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Ζεύγος ηλεκτρονίων δεσμού, Λειτουργική ομάδα, Μοναδικό ζεύγος ηλεκτρονίων, μεσομερικό φαινόμενο, αρνητικό μεσομερικό φαινόμενο, αρνητικό φαινόμενο συντονισμού, πολικότητα, θετικό μεσομερικό αποτέλεσμα, θετικό φαινόμενο συντονισμού, εφέ συντονισμού

Τι είναι το Resonance
Ο συντονισμός είναι η έννοια που περιγράφει την αλληλεπίδραση μεταξύ μοναχικών ζευγών ηλεκτρονίων και ζευγών δεσμών ηλεκτρονίων ενός μορίου που τελικά καθορίζουν τη χημική δομή αυτού του μορίου. Αυτή η επίδραση μπορεί να παρατηρηθεί σε μόρια που έχουν διπλούς δεσμούς. Ο συντονισμός των μορίων προκαλεί την πολικότητα των μορίων.
Η αλληλεπίδραση μεταξύ μεμονωμένων ζευγών ηλεκτρονίων στα άτομα και των ζευγών δεσμών ηλεκτρονίων pi παρακείμενων χημικών δεσμών οδηγεί σε συντονισμούς. Ένα μόριο μπορεί να έχει διάφορες μορφές συντονισμού ανάλογα με τον αριθμό των μοναχικών ζευγών ηλεκτρονίων και των δεσμών pi. Αλλά η πραγματική δομή του μορίου είναι ένα υβρίδιο όλων των πιθανών δομών συντονισμού.
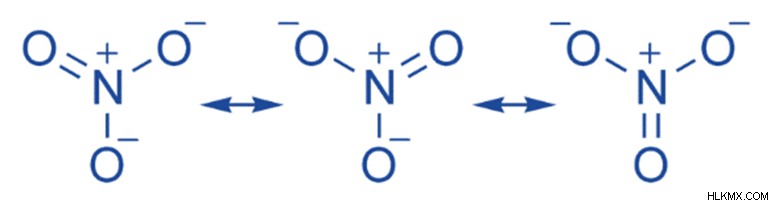
Εικόνα 1:Δομές συντονισμού του NO3
Η παραπάνω εικόνα δείχνει δομές συντονισμού νιτρικών ιόντων. Εδώ, τα μόνα ζεύγη ηλεκτρονίων στα άτομα οξυγόνου αλληλεπιδρούν με τα ηλεκτρόνια του δεσμού pi. Αυτό έχει ως αποτέλεσμα την μετεγκατάσταση ηλεκτρονίων. Η πραγματική δομή του μορίου είναι μια υβριδική δομή όλων αυτών των δομών συντονισμού.
Το φαινόμενο συντονισμού των μορίων μπορεί να εμφανιστεί σε δύο τύπους:το φαινόμενο θετικού συντονισμού και το φαινόμενο αρνητικού συντονισμού. Το φαινόμενο θετικού συντονισμού περιγράφει την μετεγκατάσταση ηλεκτρονίων σε μόρια που έχουν θετικά φορτία. Αυτό συμβαίνει για τη σταθεροποίηση των θετικών φορτίων. Το φαινόμενο αρνητικού συντονισμού περιγράφει την μετεγκατάσταση ηλεκτρονίων σε μόρια με αρνητικά φορτία. Αυτό συμβαίνει για τη σταθεροποίηση αρνητικών φορτίων.
Η υβριδική δομή που λαμβάνεται από τις δομές συντονισμού των μορίων έχει χαμηλότερη ενέργεια από αυτή όλων των δομών συντονισμού. Επομένως, η υβριδική δομή είναι η πραγματική δομή του μορίου.
Τι είναι το Mesomeric Effect
Το μεσομερές φαινόμενο είναι η σταθεροποίηση ενός μορίου με τη χρήση διαφορετικών λειτουργικών ομάδων ή υποκαταστατών. Μερικοί υποκαταστάτες είναι ομάδες δότες ηλεκτρονίων ενώ μερικοί είναι ομάδες απόσυρσης ηλεκτρονίων. Αυτό συμβαίνει λόγω της διαφοράς μεταξύ των ηλεκτραρνητικών τιμών των ατόμων σε αυτές τις ομάδες υποκαταστατών. Π.χ.:υψηλότερη η ηλεκτραρνητικότητα, μεγαλύτερη η ικανότητα δωρεάς ηλεκτρονίων.
Μερικά παραδείγματα ομάδων δωρητών ηλεκτρονίων είναι –O, -NH2 , -F, -Br, κ.λπ. Η επίδραση της δωρεάς ηλεκτρονίων ή της απελευθέρωσης αυτών των υποκαταστατών είναι γνωστή ως αρνητικό μεσομερικό φαινόμενο ή Μ-. Μερικά παραδείγματα για ομάδες απόσυρσης ηλεκτρονίων είναι –NO2 , -CN, -C=O, κ.λπ. Η επίδραση της απόσυρσης ηλεκτρονίων αυτών των υποκαταστατών είναι γνωστή ως θετικό μεσομερικό φαινόμενο ή M+.
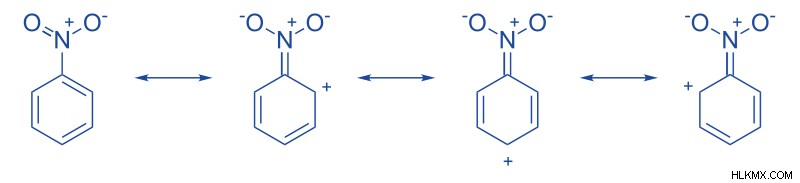
Εικόνα 2:Σταθεροποίηση νιτροβενζολίου μέσω θετικού μεσομερισμού
Σε συζευγμένα συστήματα (μόρια που έχουν εναλλασσόμενους διπλούς δεσμούς), το μεσομερικό φαινόμενο μπορεί να μετακινηθεί κατά μήκος του συστήματος. Είναι η μετεγκατάσταση των ζευγών ηλεκτρονίων του δεσμού pi. Αυτό συμβαίνει για τη σταθεροποίηση του μορίου.
Διαφορά μεταξύ συντονισμού και μεσομερικού φαινομένου
Ορισμός
Συντονισμός: Ο συντονισμός είναι η έννοια που περιγράφει την αλληλεπίδραση μεταξύ μοναχικών ζευγών ηλεκτρονίων και ζευγών ηλεκτρονίων δεσμών ενός μορίου που τελικά καθορίζει τη χημική δομή αυτού του μορίου.
Μεσομερικό εφέ: Το μεσομερές φαινόμενο είναι η σταθεροποίηση ενός μορίου με τη χρήση διαφορετικών λειτουργικών ομάδων ή υποκαταστατών.
Αιτιογόνος παράγοντας
Συντονισμός: Ο συντονισμός εμφανίζεται λόγω της παρουσίας μοναχικών ζευγών δίπλα σε διπλούς δεσμούς.
Μεσομερικό εφέ: Το μεσομερές φαινόμενο εμφανίζεται λόγω της παρουσίας υποκαταστατών/λειτουργικών ομάδων ή συζευγμένων συστημάτων.
Διαφορετικοί τύποι
Συντονισμός: Ο συντονισμός μπορεί να βρεθεί ως αποτέλεσμα θετικού συντονισμού και ως αποτέλεσμα αρνητικού συντονισμού.
Μεσομερικό εφέ: Το μεσομερικό αποτέλεσμα μπορεί να βρεθεί ως θετικό μεσομερικό αποτέλεσμα και αρνητικό μεσομερικό αποτέλεσμα.
Συμπέρασμα
Ο συντονισμός και το μεσομερικό φαινόμενο είναι δύο έννοιες που χρησιμοποιούνται για να περιγράψουν τη σταθεροποίηση των μορίων μέσω της μετεγκατάστασης ηλεκτρονίων σε όλο το μόριο. Η κύρια διαφορά μεταξύ συντονισμού και μεσομερούς φαινομένου είναι ότι ο συντονισμός εμφανίζεται λόγω της αλληλεπίδρασης μεταξύ μοναχικών ζευγών ηλεκτρονίων και ζευγών ηλεκτρονίων δεσμού, ενώ το μεσομερές αποτέλεσμα εμφανίζεται λόγω της παρουσίας ομάδων υποκατάστατων ή λειτουργικών ομάδων.