Διαφορά μεταξύ Αμφιπρωτικού και Αμφοτερικού
Κύρια διαφορά – Αμφιπρωτικό εναντίον Αμφοτερικού
Αμφοτερισμός είναι η παρουσία αμφοτερικών ιδιοτήτων. Οι αμφοτερικές ουσίες είναι ενώσεις που μπορούν να λειτουργήσουν και ως οξέα και ως βάσεις ανάλογα με το μέσο. Ο όρος αμφιπρωτικό περιγράφει μια ουσία που μπορεί να δεχτεί και να δώσει ένα πρωτόνιο ή Η. Όλες οι αμφοτερικές ουσίες είναι αμφιπρωτικές. Αλλά όλες οι αμφιπρωτικές ουσίες δεν είναι αμφοτερικές. Ορισμένα οξείδια είναι αμφοτερικά, αλλά δεν είναι αμφιπρωτικά αφού δεν μπορούν να απελευθερώσουν ή να δεχθούν πρωτόνια. Η κύρια διαφορά μεταξύ αμφιπρωτικού και αμφοτερικού είναι ότι το αμφιπρωτικό αναφέρεται στην ικανότητα δωρεάς ή αποδοχής πρωτονίων ενώ το αμφοτερικό αναφέρεται στην ικανότητα να δρα ως οξύ ή βάση.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το Αμφιπρωτικό
– Ορισμός, Ενώσεις
2. Τι είναι το Amphoteric
– Ορισμός, Ενώσεις
3. Ποια είναι η διαφορά μεταξύ Αμφιπρωτικού και Αμφοτερικού
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Οξύ, Αμφιπρωτικό, Αμφοτερικό, Αμφοτερισμός, Βάση, Ιόν Υδρονίου, Υδροξείδια, Οξείδια, Πρωτόνιο

Τι είναι το Amphiprotic
Στη χημεία, ο όρος αμφιπρωτικό περιγράφει μια ουσία που μπορεί να δεχτεί και να δώσει ένα πρωτόνιο ή ένα Η. Μια αμφιπρωτική ένωση έχει τόσο όξινες όσο και βασικές ιδιότητες και μπορεί να δράσει είτε ως οξύ ή μια βάση αφού ένα οξύ είναι ένα χημικό είδος που μπορεί να δώσει ένα πρωτόνιο ενώ μια βάση είναι μια ένωση που μπορεί να δώσει ένα ιόν υδροξυλίου (-ΟΗ) στο μέσο. Για παράδειγμα, τα αμινοξέα είναι αμφιπρωτικά μόρια. Αυτό συμβαίνει επειδή τα αμινοξέα αποτελούνται από ομάδες αμίνης (βασικές) και καρβοξυλομάδες (όξινες).
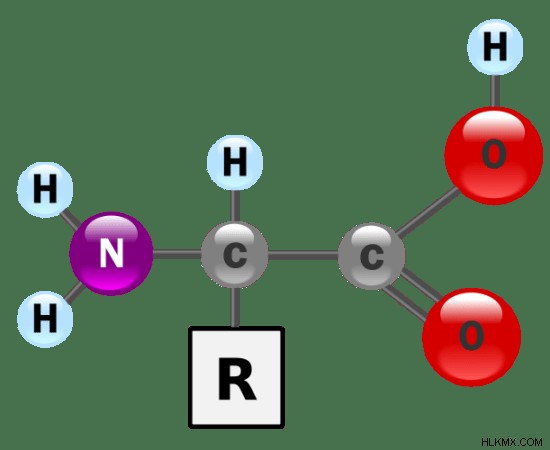
Εικόνα 1:Τα αμινοξέα αποτελούνται από μια ομάδα –NH2 και –COOH.
Μια από τις πιο σημαντικές αμφιπρωτικές ενώσεις είναι το νερό. Όταν ένα οξύ δίνει ένα πρωτόνιο στο νερό, το νερό μπορεί να δεχτεί αυτό το πρωτόνιο και να σχηματίσει ιόντα υδρονίου (H3 Ο). Όταν μια βάση αντιδρά με ένα μόριο νερού, το μόριο του νερού δίνει ένα πρωτόνιο. Η αμφιπρωτική φύση αναφέρεται στην ικανότητα τόσο της δωρεάς όσο και της αποδοχής πρωτονίων. Η αμφιπρωτική φύση του νερού περιγράφει την ικανότητα του νερού να είναι αμφιπρωτικό.
Τι είναι το Amphoteric
Το αμφοτερικό αναφέρεται στην ικανότητα να δρα τόσο ως οξύ όσο και ως βάση. Η συμπεριφορά αυτών των ενώσεων εξαρτάται από το μέσο. Το νερό είναι ένα καλό παράδειγμα αμφοτερικής ουσίας. Τα μόρια του νερού μπορούν να απελευθερώσουν πρωτόνια ή να δέχονται πρωτόνια και μπορούν να λειτουργήσουν ως οξύ ή βάση. Το μοναχικό ζεύγος στο άτομο οξυγόνου του μορίου του νερού βοηθά στην αποδοχή ενός εισερχόμενου πρωτονίου.
Αμφοτερική φύση σημαίνει ότι έχετε αμφοτερικές ιδιότητες. Τα περισσότερα από τα οξείδια και τα υδροξείδια είναι καλά παραδείγματα αυτών των ουσιών. Ένα αμφοτερικό οξείδιο είναι ένα οξείδιο που μπορεί να δράσει είτε ως οξύ είτε ως βάση σε μια αντίδραση για την παραγωγή άλατος και νερού. Ο αμφοτερισμός εξαρτάται από την κατάσταση οξείδωσης των ατόμων στο οξείδιο ή το υδροξείδιο. Δεδομένου ότι τα περισσότερα μέταλλα έχουν πολλαπλές καταστάσεις οξείδωσης, μπορούν να σχηματίσουν αμφοτερικά οξείδια και υδροξείδια.

Εικόνα 2:Το οξείδιο του ψευδαργύρου είναι ένα αμφοτερικό οξείδιο
Για παράδειγμα, το οξείδιο του ψευδαργύρου είναι ένα αμφοτερικό οξείδιο. Μπορεί να αντιδράσει τόσο με οξέα όσο και με βάσεις. Όταν αντιδρά με θειικό οξύ, το οξείδιο του ψευδαργύρου σχηματίζει τον θειικό ψευδάργυρο και το νερό ως τελικά προϊόντα. Όταν το οξείδιο του ψευδαργύρου αντιδρά με υδροξείδιο του νατρίου (υδατικό), ψευδάργυρο νάτριο (Na2 [Zn(OH)4 ]) σχηματίζεται. Όταν λαμβάνονται υπόψη τα υδροξείδια, το υδροξείδιο του αργιλίου και το υδροξείδιο του βηρυλλίου είναι τα πιο κοινά αμφοτερικά υδροξείδια.
Διαφορά μεταξύ Αμφιπρωτικού και Αμφοτερικού
Ορισμός
Αμφίπρωτο: Ο όρος αμφιπρωτικό περιγράφει μια ουσία που μπορεί να δεχτεί και να δώσει ένα πρωτόνιο ή H.
Αμφίπρωτο: Ο όρος αμφοτερικό αναφέρεται στην ικανότητα να δρα τόσο ως οξύ όσο και ως βάση.
Θεωρία
Αμφίπρωτο: Οι αμφιπρωτικές ουσίες μπορούν να δέχονται ή να δωρίζουν πρωτόνια.
Αμφίπρωτο: Οι αμφοτερικές ουσίες μπορούν να λειτουργήσουν και ως οξύ και ως βάση.
Φύση
Αμφίπρωτο: Όλες οι αμφοτερικές ουσίες είναι αμφιπρωτικές.
Αμφίπρωτο: Όλες οι αμφιπρωτικές ουσίες δεν είναι αμφοτερικές.
Συμπέρασμα
Η κύρια διαφορά μεταξύ αμφιπρωτικού και αμφοτερικού είναι ότι αμφιπρωτικό σημαίνει την ικανότητα δωρεάς ή αποδοχής πρωτονίων ενώ αμφοτερικό σημαίνει την ικανότητα να δρα ως οξύ ή βάση. Ωστόσο, όλες οι αμφιπρωτικές ουσίες δεν είναι αμφοτερικές. Ορισμένα οξείδια είναι αμφοτερικά, αλλά δεν είναι αμφιπρωτικά, καθώς δεν μπορούν να απελευθερώσουν ή να δεχθούν πρωτόνια.
Αναφορά:
1. Helmenstine, Anne Marie. "Αμφιπρωτικός ορισμός." ThoughtCo, Mar. 8, 2014, Διαθέσιμο εδώ.
2. "11.11:Amphiprotic Species." Chemistry LibreTexts, Libretexts, 6 Σεπτεμβρίου 2017, Διαθέσιμο εδώ.
3. Helmenstine, Anne Marie. "Αμφοτερικός ορισμός και παραδείγματα." ThoughtCo, Μάιος. 4, 2017, Διαθέσιμο εδώ.
Εικόνα Ευγενική προσφορά:
1. "AminoAcidball" By GYassineMrabet – δημιουργήθηκε με το Inkscape. – Ίδιο έργο (Δημόσιος Τομέας) μέσω Commons Wikimedia
2. «Δείγμα οξειδίου ψευδαργύρου» Από τον Adam Rędzikowski – Δικό έργο (CC BY-SA 4.0) μέσω Commons Wikimedia