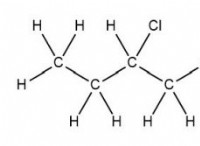
Πώς διαφέρει η ένωση από τα μόρια;
Ένωση:
- Μια ένωση είναι μια ουσία που περιέχει δύο ή περισσότερα στοιχεία που συνδέονται χημικά μαζί σε ένα σταθερό ποσοστό.
- Οι ενώσεις μπορούν να αντιπροσωπεύονται από χημικούς τύπους που υποδεικνύουν τους τύπους και τις αναλογίες των συστατικών στοιχείων.
- Κάθε ένωση έχει ένα μοναδικό σύνολο ιδιοτήτων που διαφέρουν από τις ιδιότητες των μεμονωμένων στοιχείων της.
- Οι ενώσεις μπορούν να υπάρχουν ως στερεά, υγρά ή αέρια, ανάλογα με τις φυσικές και χημικές τους ιδιότητες.
μόριο:
- Ένα μόριο είναι μια ομάδα ατόμων που συγκρατούνται από χημικούς δεσμούς. Τα μόρια μπορούν να αποτελούνται από τον ίδιο τύπο ατόμου, όπως το οξυγόνο (Ο2) ή διαφορετικούς τύπους ατόμων, όπως το νερό (H2O).
- Τα μόρια είναι οι μικρότερες μονάδες μιας ένωσης που διατηρούν τις χημικές ιδιότητες της ένωσης.
- Τα μόρια μπορούν να συνδεθούν μεταξύ τους για να σχηματίσουν μεγαλύτερες δομές, όπως κρύσταλλα, πολυμερή και βιολογικά μακρομόρια.
Η βασική διαφορά μεταξύ μιας ένωσης και ενός μορίου είναι ότι μια ένωση είναι μια συγκεκριμένη χημική ουσία, ενώ ένα μόριο είναι μια βασική μονάδα ύλης που μπορεί να υπάρχει ανεξάρτητα ή ως μέρος μιας ένωσης. Όλες οι ενώσεις αποτελούνται από μόρια, αλλά όχι όλα τα μόρια είναι ενώσεις. Για παράδειγμα, το οξυγόνο (Ο2) είναι ένα μόριο αλλά όχι μια ένωση επειδή αποτελείται από μόνο ένα είδος ατόμου.
Συνοπτικά, οι ενώσεις είναι ουσίες που αποτελούνται από δύο ή περισσότερα στοιχεία που συνδέονται χημικά μαζί, ενώ τα μόρια είναι ομάδες ατόμων που συγκρατούνται από χημικούς δεσμούς. Τα μόρια μπορούν να σχηματίσουν ενώσεις όταν διαφορετικοί τύποι ατόμων συνδυάζονται σε συγκεκριμένες αναλογίες.