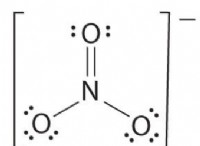
Γιατί οι μη πολικές ενώσεις είναι αδιάλυτες στο νερό;
Οι μη πολικές ενώσεις, από την άλλη πλευρά, είναι μόρια που δεν έχουν πολική δομή. Δεν έχουν θετικό τέλος ή αρνητικό τέλος, επομένως δεν προσελκύονται από μόρια νερού. Αυτή η έλλειψη έλξης σημαίνει ότι οι μη πολικές ενώσεις δεν διαλύονται στο νερό.
Ένα παράδειγμα μη πολικής ένωσης είναι το λάδι. Το πετρέλαιο είναι ένα μείγμα υδρογονανθράκων, τα οποία είναι μόρια που αποτελούνται από άτομα άνθρακα και υδρογόνου. Τα άτομα άνθρακα και υδρογόνου είναι και τα δύο μη πολικά, οπότε το πετρέλαιο δεν διαλύεται στο νερό.
Η αδυναμία των μη πολικών ενώσεων να διαλύονται στο νερό είναι σημαντική για διάφορους λόγους. Ένας λόγος είναι ότι μας επιτρέπει να διαχωρίζουμε τις μη πολικές ενώσεις από το νερό χρησιμοποιώντας μια διαδικασία που ονομάζεται εκχύλιση. Η εκχύλιση είναι μια διαδικασία στην οποία χρησιμοποιείται ένας διαλύτης για τη διάλυση μιας ένωσης που δεν είναι διαλυτή στο νερό. Ο διαλύτης στη συνέχεια διαχωρίζεται από το νερό και η ένωση ανακτάται.
Ένας άλλος λόγος για τον οποίο η ανικανότητα των μη πολικών ενώσεων να διαλύονται στο νερό είναι σημαντική είναι ότι βοηθά στη διατήρηση της δομής των ζωντανών πραγμάτων. Οι κυτταρικές μεμβράνες των ζωντανών πραγμάτων αποτελούνται από φωσφολιπιδική διπλοστοιβάδα, η οποία είναι ένα διπλό στρώμα φωσφολιπιδίων. Τα φωσφολιπίδια είναι μόρια που έχουν πολική κεφαλή και μη πολική ουρά. Οι πολικές κεφαλές των φωσφολιπιδίων αντιμετωπίζουν προς τα έξω, όπου αλληλεπιδρούν με το νερό και οι μη πολικές ουρές αντιμετωπίζουν προς τα μέσα, όπου αλληλεπιδρούν μεταξύ τους. Αυτή η διάταξη δημιουργεί ένα εμπόδιο που εμποδίζει την είσοδο των υδάτινων μορίων από την είσοδο στα κύτταρα και τα νερού-αλληλοεξαρτώμενα μόρια.