Γιατί οι κορεσμένες αλειφατικές ενώσεις έχουν μεμονωμένους δεσμούς;
* Αλειμιτικές ενώσεις: Αυτοί είναι υδρογονάνθρακες (ενώσεις κατασκευασμένες μόνο από άνθρακα και υδρογόνο) που δεν περιέχουν αρωματικούς δακτυλίους. Μπορούν να είναι ανοιχτές αλυσίδες ή διακλαδισμένες δομές.
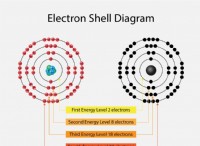
* Κορεσμένο: Αυτό σημαίνει ότι κάθε άτομο άνθρακα στην ένωση έχει σχηματίσει τον μέγιστο αριθμό δεσμών που είναι δυνατόν με άτομα υδρογόνου. Ο άνθρακας έχει τέσσερα ηλεκτρόνια σθένους και σε μια κορεσμένη ένωση, και τα τέσσερα από αυτά τα ηλεκτρόνια εμπλέκονται σε μεμονωμένους δεσμούς είτε με άλλα άνθρακα είτε με άτομα υδρογόνου.
Γιατί δεν υπάρχουν διπλά ή τριπλά ομόλογα;
* Η χωρητικότητα συγκόλλησης του άνθρακα: Ο άνθρακας μπορεί να σχηματίσει τέσσερις δεσμούς. Σε μια κορεσμένη ένωση, και οι τέσσερις από αυτούς τους δεσμούς χρησιμοποιούνται για μεμονωμένους δεσμούς, αφήνοντας κανένα περιθώριο για διπλούς ή τριπλούς δεσμούς.
* Η ικανότητα συγκόλλησης του υδρογόνου: Το υδρογόνο μπορεί να σχηματίσει μόνο έναν δεσμό. Σε μια κορεσμένη ένωση, κάθε άτομο υδρογόνου σχηματίζει ήδη έναν μόνο δεσμό με άτομο άνθρακα.
Παράδειγμα:
* Το αιθάνιο (C₂H₆) είναι μια κορεσμένη αλειφατική ένωση. Κάθε άτομο άνθρακα σχηματίζει τέσσερις μεμονωμένους δεσμούς:ένα με τον άλλο άνθρακα και τρία με άτομα υδρογόνου.
Σε αντίθεση:
* Οι ακόρεστες αλειφατικές ενώσεις έχουν διπλούς ή τριπλούς δεσμούς μεταξύ ατόμων άνθρακα, πράγμα που σημαίνει ότι δεν μπορούν να είναι πλήρως κορεσμένα με υδρογόνο. Παραδείγματα περιλαμβάνουν αιθένιο (C₂H₄) με διπλό δεσμό και Athyne (C₂H₂) με τριπλό δεσμό.
Επιτρέψτε μου να ξέρω αν έχετε περισσότερες ερωτήσεις!