Πώς αποδεικνύετε ότι το υγρό που συλλέγεται είναι νερό;
1. Φυσικές ιδιότητες:
* σημείο βρασμού: Το νερό βράζει στους 100 ° C (212 ° F) σε τυπική ατμοσφαιρική πίεση. Ζεσταίνετε το υγρό και παρατηρήστε τη θερμοκρασία στην οποία βράζει. Εάν βράζει στους ή πολύ κοντά στους 100 ° C, είναι ένας ισχυρός δείκτης νερού.
* Σημείο κατάψυξης: Το νερό παγώνει στους 0 ° C (32 ° F). Τοποθετήστε το υγρό σε καταψύκτη και παρατηρήστε εάν στερεοποιείται σε ή γύρω από αυτή τη θερμοκρασία.
* Πυκνότητα: Το νερό έχει πυκνότητα περίπου 1 g/ml στους 4 ° C. Μπορείτε να μετρήσετε τον όγκο του υγρού και τη μάζα του. Εάν η πυκνότητα είναι κοντά σε 1 g/ml, υποστηρίζει τη δυνατότητα νερού.
2. Χημικές δοκιμές:
* χαρτί Litmus: Το νερό είναι ουδέτερο, που σημαίνει ότι δεν είναι ούτε όξινο ούτε βασικό. Βυθίστε το χαρτί Litmus στο υγρό. Δεν πρέπει να αλλάζει χρώμα, υποδεικνύοντας την ουδετερότητα.
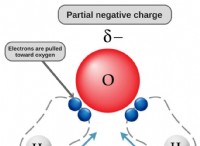
* Άνυδρο θειικό χαλκό: Το άνυδρο θειικό χαλκό είναι μια λευκή σκόνη. Όταν έρχεται σε επαφή με το νερό, γίνεται μπλε. Προσθέστε μια μικρή ποσότητα υγρού σε ένα δείγμα άνυδρου θειικού χαλκού. Εάν γίνει μπλε, επιβεβαιώνει την παρουσία νερού.
* Χλωρίδιο κοβαλτίου: Το χαρτί χλωριούχου κοβαλτίου είναι μπλε όταν στεγνώσει. Γυρίζει ροζ παρουσία νερού. Βυθίστε ένα κομμάτι χαρτιού χλωριούχου κοβαλτίου στο υγρό. Εάν αλλάξει σε ροζ, έχετε νερό.
3. Άλλοι δείκτες:
* γεύση και οσμή: Το νερό έχει χαρακτηριστική γεύση και είναι άοσμο. Να είστε προσεκτικοί με αυτό το τεστ, καθώς ορισμένες μολυντές μπορεί να έχουν παρόμοια γεύση ή οσμή.
* εμφάνιση: Το νερό είναι γενικά καθαρό και διαφανές. Σημειώστε οποιοδήποτε χρώμα ή θολότητα.
Σημαντικές εκτιμήσεις:
* Καθαρότητα: Οι παραπάνω δοκιμές μπορούν να επιβεβαιώσουν την παρουσία νερού, αλλά δεν μπορούν να εγγυηθούν την καθαρότητα του νερού. Για πολύ καθαρό νερό, ενδέχεται να χρειαστούν πρόσθετες δοκιμές.
* Ασφάλεια: Κατά τη διεξαγωγή χημικών δοκιμών, φορούν πάντα τα κατάλληλα εργαλεία ασφαλείας και ακολουθούν τις κατάλληλες εργαστηριακές διαδικασίες.
Για μια οριστική απάντηση, ίσως χρειαστεί να χρησιμοποιήσετε ένα συνδυασμό αυτών των δοκιμών.
Σημείωση: Εάν δεν είστε σίγουροι για την προέλευση ή την ασφάλεια του υγρού, είναι πάντα καλύτερο να σφάλλετε από την πλευρά της προσοχής και να αποφύγετε την κατάποση ή την άμεση δοκιμή. Συμβουλευτείτε έναν επαγγελματία για αξιόπιστες συμβουλές αναγνώρισης και ασφάλειας.