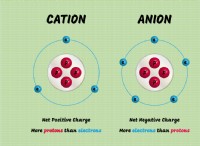
Πώς ιονίζει το οξυγόνο χάνοντας ηλεκτρόνια;
* Ηλεκτρονική διαμόρφωση του οξυγόνου: Το οξυγόνο διαθέτει 8 ηλεκτρόνια, με τη διαμόρφωση 1S2 2S2 2P⁴. Αυτό σημαίνει ότι διαθέτει 6 ηλεκτρόνια σθένους (στο εξωτερικό κέλυφος), αφήνοντάς το 2 ηλεκτρόνια κοντά σε πλήρη οκτάδα (σταθερή κατάσταση).
* Ηλεκτρική αρνητικότητα: Το οξυγόνο είναι εξαιρετικά ηλεκτροαρνητικό, που σημαίνει ότι έχει έντονη τάση να προσελκύει ηλεκτρόνια.
Διαδικασία ιονισμού:
Για να επιτευχθεί μια σταθερή διαμόρφωση, το οξυγόνο κερδίζει εύκολα 2 ηλεκτρόνια για να σχηματίσει ένα ιόν οξειδίου (O2⁻). Αυτή η διαδικασία ονομάζεται μείωση , καθώς το οξυγόνο κερδίζει ηλεκτρόνια.
Παράδειγμα:
* Atom Oxygen (O): 1S² 2S² 2P⁴
* ιόν οξειδίου (o²⁻): 1S² 2S² 2P⁶
Σημείωση: Ενώ είναι δυνατόν να απομακρυνθούν τα ηλεκτρόνια από το οξυγόνο για να δημιουργηθούν ένα κατιόν (o⁺, o²⁺, κλπ.), Αυτό απαιτεί σημαντική ενέργεια και δεν αποτελεί κοινό φαινόμενο σε τυπικές χημικές αντιδράσεις.