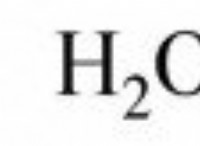Είναι το νιτρικό οξείδιο ή ο ομοιοπολικός δεσμός;
* ομοιοπολικός δεσμός: Τόσο τα άτομα αζώτου και οξυγόνου μοιράζονται ηλεκτρόνια για να σχηματίσουν τον δεσμό. Αυτή η κοινή χρήση είναι το καθοριστικό χαρακτηριστικό ενός ομοιοπολικού δεσμού.
* Dative Component: Το άτομο αζώτου συνεισφέρει και τα δύο ηλεκτρόνια στον δεσμό. Το οξυγόνο διαθέτει ένα μοναδικό ζεύγος ηλεκτρονίων που δεν εμπλέκονται στη συγκόλληση. Αυτή η "δωρεά" ηλεκτρονίων από ένα άτομο στο κοινό ζευγάρι κάνει τον δεσμό κάπως dative στη φύση.
Γιατί είναι σημαντικό να κατανοήσουμε το dative component;
Το dative συστατικό στον δεσμό ΝΟ συμβάλλει στις μοναδικές ιδιότητες του μορίου. Οδηγεί σε:
* Ο περίεργος αριθμός ηλεκτρονίων: Το NO έχει συνολικά 11 ηλεκτρόνια σθένους, καθιστώντας το ριζοσπαστικό.
* Ισχυρό παραμαγνητισμό: Το μη ζευγαρωμένο ηλεκτρόνιο δεν κάνει έντονα παραμαγνητικό.
* Αντιδραστικότητα: Το περίεργο ηλεκτρόνιο και το dative συστατικό συμβάλλουν στην υψηλή αντιδραστικότητα του ΝΟ.
Συνοπτικά: Ενώ ο δεσμός στο νιτρικό οξείδιο είναι κατά κύριο λόγο ομοιοπολικό, το συστατικό dative διαδραματίζει σημαντικό ρόλο στα χαρακτηριστικά του μορίου.