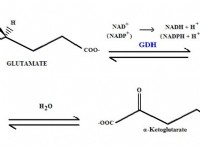
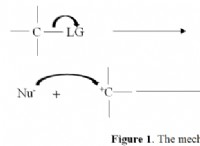
Είναι τα αντιδραστήρια των αντιδράσεων φωτός;
* νερό (h₂o) :Αυτή είναι η πηγή ηλεκτρονίων και πρωτονίων που χρησιμοποιούνται στις αντιδράσεις φωτός.
* Φωτιστική ενέργεια (φωτόνια) :Αυτή είναι η πηγή ενέργειας που οδηγεί ολόκληρη τη διαδικασία.
Βασικά σημεία που πρέπει να θυμάστε:
* Το διοξείδιο του άνθρακα (CO₂) δεν είναι αντιδραστήριο στις φωτεινές αντιδράσεις. Είναι ένα αντιδραστήριο στον κύκλο Calvin, ο οποίος είναι το δεύτερο στάδιο της φωτοσύνθεσης.
* Οξυγόνο (O₂) είναι προϊόν των αντιδράσεων φωτός , παράγεται όταν το νερό χωρίζεται για να παρέχει ηλεκτρόνια.
Συνοπτικά: Οι αντιδράσεις φωτός χρησιμοποιούν φωτεινή ενέργεια και νερό για να παράγουν ΑΤΡ, NADPH και οξυγόνο ως υποπροϊόντα. Αυτά τα προϊόντα στη συνέχεια χρησιμοποιούνται στον κύκλο Calvin για να μετατρέψουν το διοξείδιο του άνθρακα σε ζάχαρη.