Ποιο είναι το ρΗ ενός χλωριούχου υδρογόνου 0.0000001 m στο νερό;
Κατανόηση των εννοιών
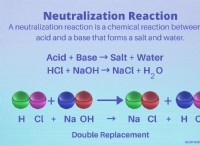
* Το HCl είναι ένα ισχυρό οξύ: Αυτό σημαίνει ότι εντελώς ιονίζει στο νερό, που σημαίνει ότι κάθε μόριο HCl διασπάται σε ένα ιόν υδρογόνου (Η) και ένα ιόν χλωριούχου (CL⁻).
* ph: Ένα μέτρο της οξύτητας ή της αλκαλικότητας ενός διαλύματος. Υπολογίζεται χρησιμοποιώντας τον τύπο:ph =-log [h⁺]
* Ένα χαμηλό ρΗ υποδηλώνει υψηλή συγκέντρωση ιόντων Η (όξινο)
* Ένα υψηλό ρΗ υποδηλώνει χαμηλή συγκέντρωση ιόντων Η (αλκαλικό/βασικό)
Υπολογισμός
1. Προσδιορίστε το [h⁺]: Δεδομένου ότι το HCl είναι ένα ισχυρό οξύ, η συγκέντρωση ιόντων Η είναι ίση με την αρχική συγκέντρωση του HCl:[H⁺] =1 x 10⁻⁷ M.
2. Υπολογίστε το ph:
ph =-log [h⁺]
ph =-log (1 x 10⁻⁷)
ph =7
Σημαντική σημείωση: Αυτός ο υπολογισμός παράγει ένα ρΗ 7, το οποίο είναι ουδέτερο. Ωστόσο, το καθαρό νερό έχει επίσης pH του 7. Στην πραγματικότητα, το ρΗ ενός διαλύματος 1 x 10 ° m του HCl θα ήταν ελαφρώς μικρότερο από 7 λόγω της πολύ μικρής συμβολής των ιόντων Η από τον αυτοροϊσμό του νερού.
Επομένως, το ρΗ ενός διαλύματος υδρογόνου 0,000000 m του υδρογόνου στο νερό είναι ουσιαστικά ουδέτερο, αλλά ελαφρώς όξινο.