Η ενέργεια δεσμού του μορίου υδρογόνου;
Αυτό σημαίνει ότι χρειάζονται 436 kilojoules ενέργειας για να σπάσουν ένα mole των δεσμών Η σε μεμονωμένα άτομα υδρογόνου.
Αυτό σημαίνει ότι χρειάζονται 436 kilojoules ενέργειας για να σπάσουν ένα mole των δεσμών Η σε μεμονωμένα άτομα υδρογόνου.
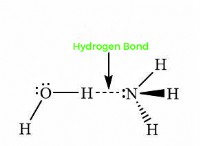
Με απλά λόγια, ο δεσμός υδρογόνου είναι ο σχηματισμός δεσμών υδρογόνου. Εμφανίζεται κυρίως μεταξύ ενός ηλεκτραρνητικού και ενός ατόμου υδρογόνου. Μερικά από τα κοινά ηλεκτραρνητικά άτομα είναι το φθόριο, το χλώριο και το οξυγόνο. Σε σύγκριση με τον ομοιοπολικό ή ιοντικό δεσμό, ο δεσμός υδρογόνου είν

Η κύρια διαφορά μεταξύ της αλυσίδας μεταφοράς ηλεκτρονίων σε προκαρυώτες και ευκαρυώτες είναι ότι η αλυσίδα μεταφοράς ηλεκτρονίων των προκαρυωτικών εμφανίζεται στην πλασματική μεμβράνη ενώ η αλυσίδα μεταφοράς ηλεκτρονίων των ευκαρυωτών εμφανίζεται στην εσωτερική μεμβράνη των μιτοχονδρίων. Οι αλυσίδ

Στη χημεία, η μοριακή αγωγιμότητα είναι η αγωγιμότητα ενός όγκου διαλύματος που περιέχει 1 mole διαλυμένου ηλεκτρολύτη, όταν τοποθετείται μεταξύ δύο παράλληλων ηλεκτροδίων. Τι είναι η Μοριακή αγωγιμότητα; Η μοριακή αγωγιμότητα μπορεί να ονομαστεί ως η ιδιότητα αγωγιμότητας ή η αγώγιμη ισχύς όλων τ