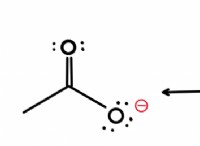
Ένωση που σχηματίζει ιόντα υδροξειδίου σε διάλυμα;
Ακολουθούν μερικά παραδείγματα:
* μεταλλικά υδροξείδια: Αυτές είναι ιοντικές ενώσεις που περιέχουν μεταλλικό κατιόν και ανιόν υδροξειδίου (ΟΗ-). Παραδείγματα περιλαμβάνουν υδροξείδιο του νατρίου (NAOH), υδροξείδιο του καλίου (ΚΟΗ) και υδροξείδιο του ασβεστίου (Ca (OH) 2).
* Ορισμένα μη μεταλλικά οξείδια: Ορισμένα μη μεταλλικά οξείδια αντιδρούν με νερό για να σχηματίσουν οξέα, τα οποία στη συνέχεια απελευθερώνουν ιόντα υδροξειδίου. Για παράδειγμα, το διοξείδιο του θείου (SO2) αντιδρά με νερό για να σχηματίσει θειώδες οξύ (H2SO3), το οποίο στη συνέχεια απελευθερώνει ιόντα υδροξειδίου.
* υδροξείδιο αμμωνίου (NH4OH): Αν και δεν είναι αληθινό υδροξείδιο, το υδροξείδιο του αμμωνίου είναι μια ασθενής βάση που σχηματίζει ιόντα αμμωνίου (NH4+) και ιόντα υδροξειδίου (ΟΗ-) σε διάλυμα.
Η ικανότητα μιας ένωσης να σχηματίζει ιόντα υδροξειδίου σε διάλυμα είναι αυτό που την καθιστά βάση. Οι βάσεις χαρακτηρίζονται από την ολισθηρή αίσθηση τους, την πικρή γεύση και την ικανότητα εξουδετερωμένων οξέων.