Γιατί η υδραζίνη είναι πιο βασική από την αμμωνία;
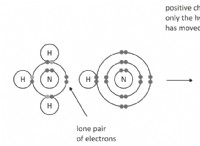
* πυκνότητα ηλεκτρονίων: Τα άτομα αζώτου τόσο στην υδραζίνη όσο και στην αμμωνία έχουν ένα μοναδικό ζεύγος ηλεκτρονίων, το οποίο είναι υπεύθυνο για την βασικότητά τους. Ωστόσο, στην υδραζίνη, η πυκνότητα ηλεκτρονίων στο άτομο αζώτου είναι ελαφρώς χαμηλότερη Λόγω της παρουσίας του δεύτερου ατόμου αζώτου, το οποίο μπορεί να αποσύρει κάποια πυκνότητα ηλεκτρονίων μέσω του δεσμού Ν-Ν.
* Επαγωγικό αποτέλεσμα: Η επίδραση του ηλεκτρονίου-μελαγχολικού του δεύτερου αζώτου στην υδραζίνη, γνωστή ως επαγωγική επίδραση, αποδυναμώνει την πυκνότητα των ηλεκτρονίων στο άτομο αζώτου, καθιστώντας λιγότερο πιθανό να δώσει το μοναδικό ζεύγος ηλεκτρονίων και να δρα ως βάση.
* τιμές pka: Οι τιμές ΡΚΑ των συζευγμένων οξέων αυτών των ενώσεων υποστηρίζουν περαιτέρω αυτή την παρατήρηση. Το ΡΚΑ του ιόντος αμμωνίου (NH₄⁺) είναι 9,25, ενώ το ΡΚΑ του ιόντος υδραζινίου (N₂H₅⁺) είναι 8,1. Ένα υψηλότερο PKA υποδεικνύει ένα ασθενέστερο οξύ, το οποίο σημαίνει ότι η αντίστοιχη βάση (αμμωνία σε αυτή την περίπτωση) είναι ισχυρότερη.
Επομένως, η αμμωνία είναι πιο βασική από την υδραζίνη.
Είναι σημαντικό να θυμόμαστε ότι η δύναμη μιας βάσης εξαρτάται από την ικανότητά του να δωρίζει ηλεκτρόνια και να σχηματίζει έναν δεσμό με ένα πρωτόνιο (H⁺). Ενώ τόσο η αμμωνία όσο και η υδραζίνη έχουν ένα μοναδικό ζεύγος ηλεκτρονίων, η πυκνότητα των ηλεκτρονίων και η επαγωγική επίδραση στην υδραζίνη καθιστούν λιγότερο αποτελεσματική στη δωρεά αυτών των ηλεκτρονίων και τη δράση ως βάση.