Ορίστε ένα μολύβι μιας ουσίας που εφαρμόζεται στην ατομική δομή;
Ένα mole σε ατομική δομή
Ένα μολύβι μιας ουσίας, στο πλαίσιο της ατομικής δομής, αντιπροσωπεύει έναν συγκεκριμένο αριθμό ατόμων ή μορίων .
Εδώ είναι η κατανομή:
* αριθμός Avogadro: Ένα mole ορίζεται ως η ποσότητα ουσίας που περιέχει τόσες στοιχειώδεις οντότητες (άτομα, μόρια, ιόντα κ.λπ.) καθώς υπάρχουν άτομα σε 0,012 χιλιόγραμμο άνθρακα-12. Αυτός ο αριθμός είναι γνωστός ως αριθμός Avogadro, ο οποίος είναι περίπου 6.022 x 10^23 οντότητες ανά mole .
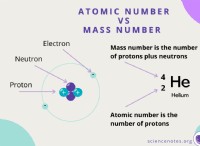
* Μονάδες ατομικής μάζας: Κάθε στοιχείο έχει μια συγκεκριμένη ατομική μάζα, που μετράται σε μονάδες ατομικής μάζας (AMU). Ένα AMU είναι περίπου ίσο με τη μάζα ενός πρωτονίου ή νετρονίου.
* Μοριακή μάζα: Η μοριακή μάζα ενός στοιχείου είναι η μάζα ενός γραμμομόρου αυτού του στοιχείου, που εκφράζεται σε γραμμάρια ανά mole (g/mol). Αυτό είναι αριθμητικά ίσο με την ατομική μάζα του στοιχείου.
Παράδειγμα:
Ας εξετάσουμε τον άνθρακα:
* Ατομική μάζα άνθρακα: 12.01 AMU
* Μοριακή μάζα άνθρακα: 12.01 g/mol
Αυτό σημαίνει:
* Ένα mole ατόμων άνθρακα ζυγίζει 12,01 γραμμάρια.
* Ένα mole ατόμων άνθρακα περιέχει 6.022 x 10^23 άτομα άνθρακα.
Σημασία στην ατομική δομή:
Η έννοια του mole είναι απαραίτητη για την κατανόηση της ατομικής δομής και των χημικών αντιδράσεων. Μας επιτρέπει να:
* Υπολογίστε τον αριθμό των ατόμων ή των μορίων σε μια δεδομένη μάζα ουσίας.
* Προσδιορίστε τη μάζα ενός συγκεκριμένου αριθμού ατόμων ή μορίων .
* Σχετικά με τη μάζα των αντιδραστηρίων και των προϊόντων σε χημικές αντιδράσεις (στοιχειομετρία).
Στην ουσία, το mole λειτουργεί ως γέφυρα μεταξύ του μικροσκοπικού κόσμου των ατόμων και των μορίων και του μακροσκοπικού κόσμου που βιώνουμε, επιτρέποντάς μας να κατανοήσουμε και να ποσοτικοποιήσουμε τις χημικές διεργασίες.