Τι αντιδρά με το αλάτι;
1. Νερό:
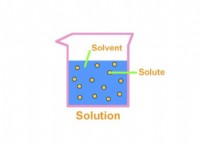
* Το αλάτι διαλύεται στο νερό, σχηματίζοντας ιόντα (Na+ και Cl-). Αυτή η διαδικασία ονομάζεται διάσπαση .
2. Οξέα:
* Το αλάτι αντιδρά με ισχυρά οξέα όπως HCl ή H2SO4 για να σχηματίσουν νέα άλατα και να απελευθερώσουν αέριο υδρογόνου (HCl). Για παράδειγμα:
* NaCl + HCl → NaCl + H2O
* NaCl + H2SO4 → Na2SO4 + 2HCL
3. Βάσεις:
* Το αλάτι αντιδρά με ισχυρές βάσεις όπως το NaOH ή το KOH για να σχηματίσουν νέα άλατα και νερό. Για παράδειγμα:
* NaCl + NaOH → NaOH + NaCl
* NACL + KOH → KCL + NAOH
4. Μέταλλα:
* Το αλάτι μπορεί να αντιδράσει με ορισμένα ενεργά μέταλλα όπως το λίθιο (Li) ή το κάλιο (k) για να σχηματίσει νέα άλατα και να απελευθερώσει αέριο υδρογόνου. Για παράδειγμα:
* 2NACL + 2LI → 2LICL + H2
5. Άλλα άλατα:
* Το αλάτι μπορεί να αντιδράσει με άλλα άλατα για να σχηματίσει νέα άλατα μέσω αντιδράσεων διπλής μετατόπισης. Για παράδειγμα:
* NACL + AGNO3 → AGCL + NANA3
6. Θερμότητα:
* Όταν θερμαίνονται σε υψηλές θερμοκρασίες, το αλάτι μπορεί να αποσυντεθεί στα συστατικά του στοιχεία, το νάτριο (NA) και το χλώριο (CL2). Αυτή είναι μια πολύ δύσκολη διαδικασία, που απαιτεί ακραίες θερμοκρασίες.
Σημαντική σημείωση:
* Οι αντιδράσεις του αλατιού επηρεάζονται συχνά από παράγοντες όπως η συγκέντρωση, η θερμοκρασία και η παρουσία άλλων ουσιών.
* Δεν εμφανίζονται όλες οι αντιδράσεις εύκολα ή εντελώς. Ορισμένες αντιδράσεις μπορεί να απαιτούν συγκεκριμένες συνθήκες ή καταλύτες.