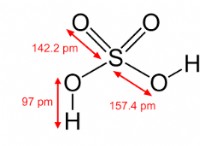
Είναι αδύναμο ή ισχυρό οργανικό οξύ;
Εδώ είναι γιατί:
* αδύναμα οξέα Μην ιονίζετε εντελώς το διάλυμα. Δωρίζουν μόνο εν μέρει τα ιόντα υδρογόνου τους (Η+).
* Ισχυρά οξέα , από την άλλη πλευρά, ιονίζει εντελώς τη λύση.
Παραδείγματα οργανικών οξέων:
* Καρβοξυλικά οξέα: Αυτοί είναι ο πιο συνηθισμένος τύπος οργανικού οξέος, με τον γενικό τύπο R-COOH, όπου R είναι ομάδα υδρογονανθράκων. Παραδείγματα περιλαμβάνουν οξικό οξύ (CH3COOH), μυρμηκικό οξύ (HCOOH) και κιτρικό οξύ (C6H8O7).
* σουλφονικά οξέα: Αυτά έχουν τη γενική φόρμουλα R-SO3H, όπου R είναι ομάδα υδρογονανθράκων. Παραδείγματα περιλαμβάνουν μεθανοσουλφονικό οξύ (CH3SO3H).
* φαινόλες: Αυτές είναι αρωματικές ενώσεις με υδροξυλική ομάδα (ΟΗ) που συνδέονται με τον αρωματικό δακτύλιο.
Γιατί τα οργανικά οξέα είναι αδύναμα;
* Η παρουσία της ομάδας υδρογονανθράκων: Η ομάδα υδρογονανθράκων που συνδέεται με την όξινη λειτουργική ομάδα (όπως το COOH ή SO3H) είναι η αποστολή ηλεκτρονίων. Αυτό καθιστά το ιόν υδρογόνου λιγότερο πιθανό να διαχωριστεί από το μόριο, με αποτέλεσμα την ασθενέστερη οξύτητα.
* Επαγωγικό αποτέλεσμα: Η επίδραση-δάνειο ηλεκτρονίων της ομάδας υδρογονανθράκων μπορεί να ενισχυθεί περαιτέρω από το επαγωγικό αποτέλεσμα, όπου τα ηλεκτρόνια ωθούν προς την όξινη λειτουργική ομάδα.
* συντονισμός: Ορισμένα οργανικά οξέα, όπως τα καρβοξυλικά οξέα, μπορούν να παρουσιάσουν δομές συντονισμού που απομακρύνουν το αρνητικό φορτίο που σχηματίζεται μετά την απώλεια ενός πρωτονίου. Αυτή η σταθεροποίηση της συζευγμένης βάσης καθιστά το οξύ ασθενέστερο.
Σημαντική σημείωση: Υπάρχουν μερικά οργανικά οξέα που θεωρούνται ισχυρότερα από άλλα. Για παράδειγμα, το τριφθοροξικό οξύ (CF3COOH) είναι ένα ισχυρό οργανικό οξύ λόγω της επίδρασης των ηλεκτρονίων που απομακρύνονται από τα άτομα φθορίου.