Πώς διαφέρει ο δεσμός σε F2 από το KCL;
f2 (αέριο φθορίου)
* Τύπος δεσμού: ομοιοπολικός δεσμός
* Αυτό σημαίνει ότι τα άτομα μοιράζονται ηλεκτρόνια για να επιτύχουν μια σταθερή διαμόρφωση ηλεκτρονίων.
* Και τα δύο άτομα φθορίου είναι εξαιρετικά ηλεκτροαρνητικά (θέλουν να κερδίσουν ηλεκτρόνια).
* Μοιράζονται ένα ζευγάρι ηλεκτρονίων εξίσου, σχηματίζοντας έναν μη πολικό ομοιοπολικό δεσμό.
KCl (χλωριούχο κάλιο)
* Τύπος δεσμού: ιονικός δεσμός
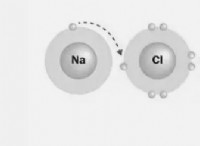
* Αυτό σημαίνει ότι ένα άτομο (κάλιο) * δωρίζει * ένα ηλεκτρόνιο σε άλλο άτομο (χλώριο) για να σχηματίσει αντίθετα φορτισμένα ιόντα.
* Το κάλιο (k) είναι ένα μέταλλο και χάνει εύκολα ένα ηλεκτρόνιο για να γίνει ένα θετικά φορτισμένο ιόν (Κ+).
* Το χλώριο (CL) είναι ένα μη μέταλλο και κερδίζει εύκολα ένα ηλεκτρόνιο για να γίνει ένα αρνητικά φορτισμένο ιόν (Cl-).
* Η έλξη μεταξύ αυτών των αντίθετα φορτισμένων ιόντων αποτελεί τον ιονικό δεσμό.
Βασικές διαφορές:
* Κοινή χρήση ηλεκτρονίων έναντι μεταφοράς: Οι ομοιοπολικοί δεσμοί μοιράζονται ηλεκτρόνια, ενώ τα ιοντικά ομόλογα μεταφέρουν ηλεκτρόνια.
* Ηλεκτροργατιστικότητα: Οι ομοιοπολικοί δεσμοί εμφανίζονται μεταξύ στοιχείων με παρόμοια ηλεκτροαρνητικότητα, ενώ οι ιοντικοί δεσμοί εμφανίζονται μεταξύ στοιχείων με πολύ διαφορετική ηλεκτροαρνητικότητα.
* πολικότητα: Οι ομοιοπολικοί δεσμοί μπορεί να είναι πολικοί ή μη πολικοί. Στο F2, ο δεσμός είναι μη πολικός, επειδή τα ηλεκτρόνια μοιράζονται εξίσου. Οι ιοντικοί δεσμοί είναι πάντα πολικοί, με θετικό και αρνητικό τέλος.
* Φυσικές ιδιότητες: Οι ομοιοπολικές ενώσεις είναι γενικά αέρια, υγρά ή στερεά χαμηλής μείωσης. Οι ιοντικές ενώσεις είναι συνήθως στερεά υψηλού επιπέδου.
Συνοπτικά: Το F2 είναι ένα μη πολικό ομοιοπολικό μόριο που συγκρατείται με την κατανομή των ηλεκτρονίων, ενώ η KCL είναι μια ιοντική ένωση που σχηματίζεται από την ηλεκτροστατική έλξη μεταξύ των αντίθετα φορτισμένων ιόντων.