Γιατί το φθόριο αντιδρά με το Xenon;
* Υψηλή ηλεκτροαρνητικότητα του φθορίου: Το φθόριο είναι το πιο ηλεκτροαρνητικό στοιχείο, που σημαίνει ότι έχει ισχυρή έλξη για τα ηλεκτρόνια. Αυτό του επιτρέπει να τραβήξει ηλεκτρόνια μακριά από το Xenon, σχηματίζοντας έναν δεσμό.
* Ενέργεια χαμηλής ιονισμού του Xenon: Το Xenon έχει σχετικά χαμηλή ενέργεια ιονισμού σε σύγκριση με άλλα ευγενή αέρια, που σημαίνει ότι χρειάζεται λιγότερη ενέργεια για να απομακρυνθεί ένα ηλεκτρόνιο από αυτό. Αυτό διευκολύνει το φθόριο να σχηματίσει έναν δεσμό με Xenon.
* Μικρό μέγεθος φθορίου: Το μικρό μέγεθος του φθορίου του επιτρέπει να προσεγγίζει στενά το άτομο Xenon και να σχηματίσει έναν ισχυρό δεσμό.
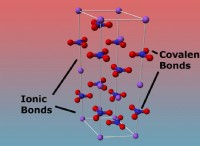
* Σχηματισμός σταθερών ενώσεων: Η αντίδραση μεταξύ φθορίου και ξενίου οδηγεί στο σχηματισμό σταθερών ενώσεων όπως το XEF2, το XEF4 και το XEF6. Αυτές οι ενώσεις έχουν ισχυρούς ομοιοπολικούς δεσμούς, οι οποίοι συμβάλλουν στη σταθερότητά τους.
Εδώ είναι μια απλοποιημένη εξήγηση:
Σκεφτείτε το έτσι:Το φθόριο είναι ένα πολύ "πεινασμένο" στοιχείο, που πάντα ψάχνει να κερδίσει ηλεκτρόνια. Το Xenon, ενώ συνήθως είναι αρκετά ευχαριστημένος με το πλήρες κέλυφος των ηλεκτρονίων, είναι ελαφρώς πιο πρόθυμη να μοιραστεί μερικά με φθόριο λόγω της σχετικά χαμηλής ενέργειας ιονισμού. Η ισχυρή έλξη μεταξύ φθορίου και ξενίου, σε συνδυασμό με την ικανότητά τους να σχηματίζουν σταθερές ενώσεις, καθιστά δυνατή αυτή την αντίδραση.
Σημαντική σημείωση: Ενώ το Xenon είναι ένα από τα λίγα ευγενή αέρια που αντιδρούν με φθόριο, δεν αντιδρά με άλλα στοιχεία ως εύκολα. Αυτό οφείλεται στο γεγονός ότι η ενέργεια του ιονισμού εξακολουθεί να είναι σχετικά υψηλή σε σύγκριση με τα περισσότερα άλλα στοιχεία.