Γιατί το νάτριο και το κάλιο υποβάλλονται σε παρόμοιες αντιδράσεις με νερό;
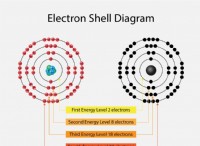
* Παρόμοια ηλεκτρονική διαμόρφωση: Τόσο το νάτριο (Na) όσο και το κάλιο (k) είναι αλκαλικά μέταλλα, που βρίσκονται στην ομάδα 1 του περιοδικού πίνακα. Αυτό σημαίνει ότι έχουν ένα ηλεκτρόνιο σθένους (ηλεκτρόνιο στο εξώτατο κέλυφος). Αυτό το ηλεκτρόνιο μεμονωμένο σθένος χάνεται εύκολα, καθιστώντας τα ιδιαίτερα αντιδραστικά.
* Ενέργειες χαμηλής ιονισμού: Λόγω της ηλεκτρονικής διαμόρφωσής τους, τόσο το νάτριο όσο και το κάλιο έχουν χαμηλές ενέργειες ιονισμού. Αυτό σημαίνει ότι απαιτεί σχετικά μικρή ενέργεια για να αφαιρέσει το ηλεκτρόνιο σθένους τους και να σχηματίσει ένα θετικό ιόν (Na+ ή K+).
* Ηλεκτροθετική φύση: Η τάση τους να χάσουν το ηλεκτρόνιο σθένους τους καθιστά εξαιρετικά ηλεκτροκίνητα. Αυτό σημαίνει ότι δίνουν εύκολα το ηλεκτρόνιο τους σε άλλα στοιχεία, όπως το οξυγόνο στο νερό.
Η αντίδραση:
Όταν το νάτριο ή το κάλιο προστίθεται στο νερό, συμβαίνει η ακόλουθη αντίδραση:
* Το άτομο του αλκαλικού μετάλλου δίνει το ηλεκτρόνιο σθένους σε ένα μόριο νερού, σχηματίζοντας ένα ιόν υδροξειδίου (ΟΗ-) και ένα άτομο υδρογόνου (Η).
* Το άτομο υδρογόνου αντιδρά με ένα άλλο μόριο νερού για να σχηματίσει ένα ιόν υδρονίου (Η3Ο+).
* Το αλκαλικό μεταλλικό ιόν (Na+ ή Κ+) διαλύεται στο νερό.
* Το απελευθερωμένο αέριο υδρογόνου (Η2) φυσαλίδες και ανάφλεξη παρουσία της θερμότητας που παράγεται από την αντίδραση.
ομοιότητες σε αντίδραση:
Οι αντιδράσεις του νατρίου και του καλίου με νερό είναι πολύ παρόμοιες λόγω των προαναφερθέντων παραγόντων:
* έντονες αντιδράσεις: Και τα δύο μέταλλα αντιδρούν βίαια με νερό, απελευθερώνοντας μεγάλη ποσότητα θερμότητας.
* σχηματισμός αερίου υδρογόνου: Και οι δύο αντιδράσεις παράγουν αέριο υδρογόνου, το οποίο είναι εξαιρετικά εύφλεκτο.
* σχηματισμός ιόντων υδροξειδίου: Και οι δύο αντιδράσεις παράγουν ιόντα υδροξειδίου, καθιστώντας τη λύση βασική.
Διαφορές:
Ενώ παρόμοια, υπάρχουν μικρές διαφορές στις αντιδράσεις:
* Αντιδραστικότητα: Το κάλιο είναι πιο αντιδραστικό από το νάτριο. Η αντίδρασή του με το νερό είναι ακόμα πιο έντονη, δημιουργώντας περισσότερη θερμότητα και μεγαλύτερη έκρηξη.
* ρυθμός αντίδρασης: Το κάλιο αντιδρά ταχύτερα με νερό από το νάτριο.
Συμπέρασμα:
Το νάτριο και το κάλιο υποβάλλονται σε παρόμοιες αντιδράσεις με νερό λόγω των παρόμοιων ηλεκτρονικών διαμορφώσεων, των ενεργειών χαμηλής ιονισμού και της ηλεκτρικής φύσης. Οι αντιδράσεις που προκύπτουν είναι εξωθερμικές, παράγουν αέριο υδρογόνου και κάνουν το διάλυμα βασικό. Αν και παρόμοιο, το κάλιο είναι πιο αντιδραστικό από το νάτριο, οδηγώντας σε μια πιο έντονη αντίδραση.