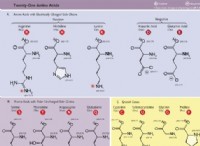
Ποιο οξύ Brønsted-Lowry έχει την ισχυρότερη συζευγμένη βάση;
Εδώ είναι γιατί:
* Brønsted-Lowry οξέα: Δωρεά πρωτόνια (Η+).
* Βάσεις συζεύξεων: Το είδος που σχηματίζεται μετά από ένα οξύ δίνει ένα πρωτόνιο.
Η σχέση: Ένα ισχυρό οξύ δίνει εύκολα το πρωτόνιο του, αφήνοντας πίσω της μια αδύναμη βάση συζυγής. Αντίθετα, ένα αδύναμο οξύ κρατάει το πρωτόνιο του πιο σφιχτά, με αποτέλεσμα μια ισχυρή συζευγμένη βάση.
Παράδειγμα:
* HCl (υδροχλωρικό οξύ): Ένα ισχυρό οξύ. Η βάση του συζευγμένου, CL- (ιόν χλωριούχου), είναι μια αδύναμη βάση.
* CH3COOH (οξικό οξύ): Ένα αδύναμο οξύ. Η συζευγμένη βάση του, CH3COOO- (οξικό ιόν), είναι μια ισχυρή βάση.
Συνοπτικά: Όσο ισχυρότερο είναι το οξύ, τόσο πιο αδύναμη είναι η συζευγμένη βάση του. Όσο πιο αδύναμο είναι το οξύ, τόσο ισχυρότερη είναι η συζευγμένη βάση του.