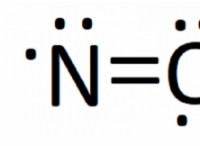Τι ισχύει για όλους τους ομοιοπολικούς δεσμούς;
* Κοινή χρήση ηλεκτρονίων: Οι ομοιοπολικοί δεσμοί σχηματίζονται όταν δύο άτομα μοιράζονται ηλεκτρόνια. Αυτή η κοινή χρήση δημιουργεί μια σταθερή διάταξη όπου και τα δύο άτομα έχουν ένα γεμάτο εξωτερικό κέλυφος.
* Μη μέταλλα: Οι ομοιοπολικοί δεσμοί συνήθως εμφανίζονται μεταξύ μη μετάλλου άτομα. Αυτό οφείλεται στο γεγονός ότι οι μη-μετάλλοι έχουν υψηλή ηλεκτροαρνητικότητα (έλξη για ηλεκτρόνια), καθιστώντας τους λιγότερο πιθανό να χάσουν ηλεκτρόνια και πιο πιθανό να τα μοιραστούν.
* Ισχυρά ομόλογα: Οι ομοιοπολικοί δεσμοί είναι γενικά strong , που σημαίνει ότι απαιτείται πολλή ενέργεια για να τα σπάσει.
* Κατευθυντική: Οι ομοιοπολικοί δεσμοί είναι κατευθυντικά , που σημαίνει ότι έχουν έναν συγκεκριμένο προσανατολισμό στο διάστημα. Αυτό οφείλεται στο γεγονός ότι τα κοινόχρηστα ηλεκτρόνια εντοπίζονται μεταξύ των δύο ατόμων.
Μερικά επιπλέον σημεία:
* Polar vs. Nonpolar: Οι ομοιοπολικοί δεσμοί μπορεί να είναι είτε πολικός ή nonpolar ανάλογα με τη διαφορά στην ηλεκτροαρνητικότητα μεταξύ των εμπλεκόμενων ατόμων.
* Πολλαπλά ομόλογα: Τα άτομα μπορούν να μοιράζονται περισσότερα από ένα ζεύγη ηλεκτρονίων, σχηματίζοντας διπλό ή τριπλό ομολογίες.
Επιτρέψτε μου να ξέρω αν θέλετε περισσότερες λεπτομέρειες σε οποιοδήποτε από αυτά τα σημεία!