Ποια αντίστοιχη συγκέντρωση ιόντων υδρονίου θα είχε ένα διάλυμα ρΗ 5;
Κατανόηση ιόντων ρΗ και υδρονίου
* ph: Ένα μέτρο της οξύτητας ή της αλκαλικότητας ενός διαλύματος. Βασίζεται στη συγκέντρωση ιόντων υδρονίου (H₃O⁺).
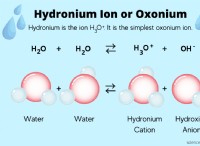
* ιόντα υδρονίου: Που σχηματίζεται όταν ένα μόριο νερού (H₂O) δέχεται ένα πρωτόνιο (H⁺) από ένα οξύ. Είναι υπεύθυνοι για τις όξινες ιδιότητες ενός διαλύματος.
Η σχέση
Η συγκέντρωση ιόντων ρΗ και υδρονίου σχετίζεται με την ακόλουθη εξίσωση:
ph =-log [h₃o⁺]
Οπου:
* ph είναι το pH του διαλύματος
* [h₃o⁺] είναι η μοριακή συγκέντρωση ιόντων υδρονίου
Υπολογισμός της συγκέντρωσης ιόντων υδρονίου
1. Αναδιατάξτε την εξίσωση:
[H₃o⁺] =10⁻ph
2. Αντικαταστήστε την τιμή pH:
[H₃o⁺] =10⁻⁵
3. Υπολογίστε:
[H₃o⁺] =1 x 10⁻⁵ m
Επομένως, ένα διάλυμα ρΗ 5 έχει συγκέντρωση ιόντων υδρονίου 1 x 10 ⁻⁵ m.