Ποιες είναι οι διαφορές μεταξύ φυσικών και χημικών αντιδράσεων;
Φυσικές αντιδράσεις:
* Αλλαγές στην εμφάνιση ή κατάσταση: Οι φυσικές αλλαγές επηρεάζουν τη μορφή ή την εμφάνιση μιας ουσίας, αλλά όχι τη χημική του σύνθεση. Είναι συνήθως αναστρέψιμα.
* Δεν σχηματίστηκαν νέες ουσίες: Η χημική μακιγιάζ των ουσιών παραμένει η ίδια.
* Οι ενεργειακές αλλαγές είναι συχνά μικρές: Η ενέργεια που εμπλέκεται σε μια φυσική αλλαγή είναι συνήθως μικρότερη από αυτή σε μια χημική αλλαγή.
* Παραδείγματα:
* Λήψη πάγου (στερεό έως υγρό)
* Διάλυση ζάχαρης σε νερό
* Σπάζοντας ένα ποτήρι
* Βραστό νερό (υγρό σε αέριο)
* Συνθλίβοντας ένα βράχο
Χημικές αντιδράσεις:
* Αλλαγές στη χημική σύνθεση: Οι χημικές αλλαγές έχουν ως αποτέλεσμα τον σχηματισμό νέων ουσιών με διαφορετικές χημικές ιδιότητες.
* Νέες ουσίες σχηματίστηκαν: Τα άτομα αναδιατάσσονται για να δημιουργήσουν νέα μόρια.
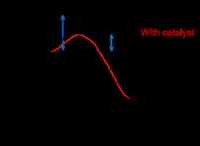
* Οι ενεργειακές αλλαγές είναι σημαντικές: Οι χημικές αντιδράσεις συχνά απελευθερώνουν ή απορροφούν σημαντικές ποσότητες ενέργειας (εξωθερμικές ή ενδοθερμικές αντιδράσεις).
* Παραδείγματα:
* Καύση ξύλου (καύση)
* Σκουριά σιδήρου (οξείδωση)
* Ψήσιμο ενός κέικ
* Χωνοποιώντας φαγητό
* Φωτοσύνθεση σε φυτά
Εδώ είναι ένας πίνακας που συνοψίζει τις βασικές διαφορές:
| Χαρακτηριστικό | Φυσική αλλαγή | Χημική αλλαγή |
| --- | --- | --- |
| Σύνθεση | Παραμένει το ίδιο | Αλλαγές |
| Νέες ουσίες που σχηματίστηκαν; | Όχι | Ναι |
| Αναστροφή | Συχνά αναστρέψιμο | Συνήθως δεν είναι αναστρέψιμο |
| Αλλαγές ενέργειας | Συχνά μικρό | Συχνά σημαντική |
| Παραδείγματα | Τήξη, κατάψυξη, βρασμό, διάλυση | Καύση, σκουριά, μαγείρεμα, φωτοσύνθεση |
Θυμηθείτε: Μερικές φορές μπορεί να είναι δύσκολο να ταξινομήσουμε μια αλλαγή ως αυστηρά φυσική ή χημική. Για παράδειγμα, η διάλυση του αλατιού στο νερό φαίνεται να είναι μια φυσική αλλαγή, αλλά περιλαμβάνει επίσης το σχηματισμό ιόντων, που είναι μια χημική αλλαγή.