Γιατί ένα αλάτι που περιέχει κατιόν από ισχυρή βάση και ένα αδύναμο οξύ ανιόν είναι βασικό διάλυμα;
Κατανόηση των εννοιών
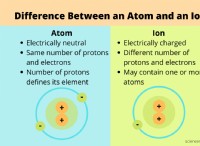
* Ισχυρές βάσεις Διαχωρίζονται πλήρως στο νερό, απελευθερώνοντας ιόντα υδροξειδίου (OH-) και κατιόν.
* αδύναμα οξέα Μόνο εν μέρει διαχωρίζονται στο νερό, απελευθερώνοντας ιόντα υδρογόνου (Η+) και ένα ανιόν. Το ανιόν ενός ασθενούς οξέος έχει την τάση να δέχεται πρωτόνια (Η+).
* υδρόλυση είναι η αντίδραση μιας ουσίας με νερό. Στην περίπτωση των αλάτων, η υδρόλυση περιλαμβάνει την αλληλεπίδραση των ιόντων του αλατιού με μόρια νερού.
Πώς το αλάτι σχηματίζει μια βασική λύση
1. Διάσπαση: Όταν το αλάτι διαλύεται στο νερό, διαχωρίζεται στο κατιόν και το ανιόν του.
2. Υδρόλυση ανιόντων: Το ανιόν από το αδύναμο οξύ αντιδρά με μόρια νερού, αποδοχή ενός πρωτονίου (Η+). Αυτή η αντίδραση παράγει ιόντα υδροξειδίου (ΟΗ-) και το μη φορτωμένο αδύναμο οξύ.
`` `
A- + h2o ⇌ ha + oh-
`` `
(Α-αντιπροσωπεύει το ανιόν του ασθενούς οξέος και το ΗΑ αντιπροσωπεύει το μη φορτωμένο αδύναμο οξύ)
3. Αυξημένη συγκέντρωση OH: Η παραγωγή ιόντων υδροξειδίου (ΟΗ-) από την υδρόλυση ανιόντων αυξάνει τη συγκέντρωση ιόντων υδροξειδίου στο διάλυμα.
4. Βασική λύση: Δεδομένου ότι η συγκέντρωση ιόντων υδροξειδίου (ΟΗ-) είναι υψηλότερη από τη συγκέντρωση ιόντων υδρογόνου (Η+), το διάλυμα γίνεται βασικό.
Παράδειγμα:
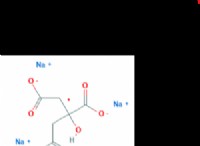
Το οξικό νάτριο (NACh3COO) είναι ένα άλας που σχηματίζεται από το ισχυρό υδροξείδιο του νατρίου (ΝΑΟΗ) και το αδύναμο οξύ οξικό οξύ (CH3COOH).
* Τα ιόντα νατρίου (Na+) από NaOH δεν αντιδρούν σημαντικά με το νερό.
* Τα ιόντα οξικού άλατος (CH3COO-) από οξικό οξύ αντιδρούν με νερό, παράγοντας ιόντα υδροξειδίου (ΟΗ-) και οξικό οξύ (CH3COOH).
Αυτή η αντίδραση οδηγεί σε αύξηση της συγκέντρωσης ιόντων υδροξειδίου, καθιστώντας το διάλυμα βασικό.
Συνοπτικά:
Τα άλατα που σχηματίζονται από μια ισχυρή βάση και ένα αδύναμο οξύ παράγουν βασικά διαλύματα επειδή το ανιόν των ασθενών υδρολύσεων οξέος, δημιουργώντας ιόντα υδροξειδίου (ΟΗ-) και αυξάνοντας το ρΗ του διαλύματος.