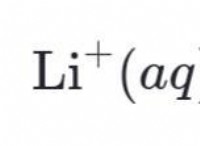Πώς είναι ένας μεταλλικός δεσμός διαφορετικός ένας ιοντικός δεσμός;
Μεταλλικοί δεσμοί
* Φύση της σύνδεσης: Οι μεταλλικοί δεσμοί περιλαμβάνουν μια "θάλασσα" των απομακρυσμένων ηλεκτρονίων. Τα άτομα μετάλλων χάνουν τα ηλεκτρόνια σθένους, τα οποία στη συνέχεια είναι ελεύθερα να κινούνται σε ολόκληρη τη δομή. Αυτή η "θάλασσα" λειτουργεί ως κόλλα που κρατάει τα θετικά φορτισμένα μεταλλικά ιόντα μαζί.
* σχηματισμός: Εμφανίζεται μεταξύ των μετάλλων.
* Ιδιότητες:
* καλοί αγωγοί θερμότητας και ηλεκτρικής ενέργειας: Τα ηλεκτρόνια ελεύθερης μετακίνησης μπορούν εύκολα να μεταφέρουν τη φόρτιση και τη θερμότητα.
* εύπλαστο και όλκιμο: Τα άτομα μπορούν να γλιστρήσουν ο ένας τον άλλον χωρίς να σπάσουν τον δεσμό, επιτρέποντας στο διαμορφωμένο μέταλλο.
* λάμψη: Τα απομακρυσμένα ηλεκτρόνια μπορούν να απορροφήσουν και να εκπέμπουν ξανά το φως, δίνοντας στα μέταλλα τη λαμπερή εμφάνισή τους.
* υψηλά σημεία τήξης και βρασμού: Οι ισχυροί μεταλλικοί δεσμοί απαιτούν πολλή ενέργεια για να σπάσουν.
ιονικοί δεσμοί
* Φύση της σύνδεσης: Οι ιοντικοί δεσμοί περιλαμβάνουν την ηλεκτροστατική έλξη μεταξύ θετικά φορτισμένων ιόντων (κατιόντων) και αρνητικά φορτισμένων ιόντων (ανιόντων). Ένα άτομο χάνει ηλεκτρόνια (σχηματίζοντας κατιόν), ενώ ένα άλλο κερδίζει ηλεκτρόνια (σχηματίζοντας ένα ανιόν).
* σχηματισμός: Εμφανίζεται μεταξύ μετάλλων και μη μεταλλικών.
* Ιδιότητες:
* Φτωχοί αγωγοί ηλεκτρικής ενέργειας στην στερεά κατάσταση: Τα ιόντα σταθεροποιούνται σε ένα άκαμπτο πλέγμα και τα ηλεκτρόνια εντοπίζονται. Διεξάγουν ηλεκτρικό ρεύμα όταν διαλύονται σε νερό ή λιωμένο.
* εύθραυστο: Οι ισχυροί ιοντικοί δεσμοί καθιστούν δύσκολο για τα ιόντα να γλιστρούν ο ένας στον άλλο, έτσι ώστε η κρυσταλλική δομή να σπάει εύκολα.
* υψηλά σημεία τήξης και βρασμού: Οι ισχυρές ηλεκτροστατικές δυνάμεις απαιτούν πολλή ενέργεια για να σπάσουν τους ιοντικούς δεσμούς.
Βασικές διαφορές
| Χαρακτηριστικό | Μεταλλικός δεσμός | Ιωνικός δεσμός |
| --- | --- | --- |
| Τύπος σύνδεσης | Απομακρυσμένα ηλεκτρόνια | Ηλεκτροστατική έλξη |
| σχηματισμός | Μεταξύ μετάλλων | Μεταξύ μετάλλων και μη μετάλλων |
| ηλεκτρόνια | Κοινόχρηστο και απομακρυσμένο | Μεταφέρθηκε από ένα άτομο σε άλλο |
| αγωγιμότητα | Καλοί αγωγοί | Κακοί αγωγοί (εκτός από το αν διαλύονται ή λιωθούν)
| Μαλλιδικότητα &ολκιμότητα | Εύπλαστο και όλκιμο | Εύθραυστο |
| Σημείο τήξης/βρασμού | Υψηλή | Υψηλή |
Παραδείγματα
* Μεταλλικός δεσμός: Νάτριο (NA), Χαλκός (Cu), Χρυσός (AU)
* Ιονικός δεσμός: Χλωριούχο νάτριο (NaCl), οξείδιο μαγνησίου (MGO), βρωμιούχο κάλιο (KBR)