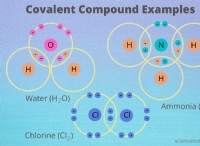
Γιατί το μόριο αμμωνίας έχει παρατηρούμενο προσανατολισμό δεσμού;
1. υβριδισμός: Το άζωτο, το κεντρικό άτομο στην αμμωνία, υφίσταται υβριδοποίηση SP³. Αυτό σημαίνει ότι τα 2s τροχιακά και τρία τροχιακά 2P συνδυάζονται για να σχηματίσουν τέσσερα νέα υβριδικά τροχιακά. Αυτά τα υβριδικά τροχιακά SP³ είναι προσανατολισμένα τετραεδρικά, με γωνίες δεσμού κοντά σε 109,5 °.
2. Lone Pair: Το άζωτο έχει ένα μοναδικό ζεύγος ηλεκτρονίων εκτός από τα τρία ζεύγη συγκόλλησης με τα άτομα υδρογόνου. Αυτό το μοναδικό ζευγάρι καταλαμβάνει ένα από τα υβριδικά τροχιακά SP³.
3. Το μοναδικό ζεύγος ηλεκτρονίων στην υβριδική τροχιά SP³ ασκεί μεγαλύτερη απόρριψη από τα ζεύγη συγκόλλησης. Αυτή η απόρριψη ωθεί τους τρεις δεσμούς Ν-Η πιο κοντά, με αποτέλεσμα μια γωνία δεσμού 107,3 ° αντί για την ιδανική τετραεδρική γωνία 109,5 °.
4. Μοριακή γεωμετρία: Το σχήμα του μορίου αμμωνίας είναι τριγωνική πυραμιδική , όχι τετραεδρικό. Αυτό οφείλεται στο γεγονός ότι το μοναδικό ζεύγος δεν θεωρείται μέρος του μοριακού σχήματος. Οι τρεις δεσμοί Ν-Η αποτελούν τη βάση της πυραμίδας, με το άτομο αζώτου στην κορυφή.
Επομένως, ο παρατηρούμενος προσανατολισμός δεσμού στην αμμωνία είναι συνέπεια:
* υβριδισμός SP³: που οδηγεί σε τετραεδρική διάταξη ζευγών ηλεκτρονίων γύρω από το άζωτο.
* Απομάκρυνση ζεύγους: που στρεβλώνει την ιδανική τετραεδρική γεωμετρία.
* Μοριακό σχήμα: η οποία καθορίζεται μόνο από τις θέσεις των ζευγών συγκόλλησης, οδηγώντας σε τριγωνική πυραμιδική δομή.