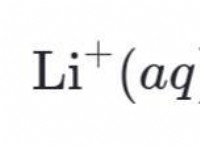Είναι το HF βάση ή οξύ;
Εδώ είναι γιατί:
* δεσμός υδρογόνου: Το HF σχηματίζει ισχυρούς δεσμούς υδρογόνου, καθιστώντας δύσκολο το ιόν υδρογόνου (Η+) να διαχωριστεί σε διάλυμα. Αυτό περιορίζει την ικανότητά του να δωρίζει πρωτόνια, ένα καθοριστικό χαρακτηριστικό των οξέων.
* Ηλεκτροργατιστικότητα: Το φθόριο είναι εξαιρετικά ηλεκτροαρνητικό, που σημαίνει ότι προσελκύει έντονα ηλεκτρόνια. Αυτό τραβάει την πυκνότητα ηλεκτρονίων μακριά από το άτομο υδρογόνου, εξασθενίζοντας τον δεσμό H-F, αλλά δεν το σπάει πλήρως.
* Ισορροπία: Το HF ιονίζει σε μικρό βαθμό στο νερό:
Hf (aq) ⇌ h + (aq) + f- (aq)
Η ισορροπία βρίσκεται πολύ προς τα αριστερά, υποδεικνύοντας ότι η πλειονότητα των μορίων HF παραμένει αδιάφορη, καθιστώντας το αδύναμο οξύ.
Βασικά σημεία:
* αδύναμα οξέα Μην ιονίζετε πλήρως τη λύση, πράγμα που σημαίνει ότι μόνο μερικώς δωρίζουν πρωτόνια.
* Ισχυρά οξέα πλήρως ιονίζουμε τη λύση, δωρίζοντας όλα τα πρωτόνια τους.
Ενώ το HF θεωρείται αδύναμο οξύ, εξακολουθεί να είναι διαβρωτικό και πρέπει να αντιμετωπίζεται με προσοχή.