Γιατί δεν υπάρχει ομοιοπολικός δεσμός σε υγρό;
* Οι ομοιοπολικοί δεσμοί είναι ισχυροί: Διατηρούν τα άτομα μαζί μέσα σε μόρια. Αυτοί οι δεσμοί δεν σπάζουν όταν μια ουσία αλλάζει από ένα στερεό σε ένα υγρό.
* Τα υγρά έχουν διαμοριακές δυνάμεις: Ενώ οι ομοιοπολικοί δεσμοί συγκρατούν τα άτομα μαζί * μέσα στα * μόρια, τα υγρά έχουν δυνάμεις * μεταξύ * μορίων. Αυτές ονομάζονται διαμοριακές δυνάμεις, όπως η σύνδεση υδρογόνου, οι αλληλεπιδράσεις διπολικής-δίπολης και οι δυνάμεις διασποράς του Λονδίνου. Αυτές οι δυνάμεις είναι ασθενέστερες από τους ομοιοπολικούς δεσμούς, γι 'αυτό τα υγρά μπορούν να ρέουν.
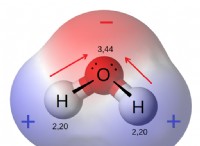
* Παράδειγμα: Το νερό είναι υγρό σε θερμοκρασία δωματίου. Έχει ισχυρούς ομοιοπολικούς δεσμούς στο H 2 O Μόρια, αλλά είναι οι δεσμοί υδρογόνου μεταξύ των μορίων νερού που του δίνουν τις υγρές του ιδιότητες.
Εδώ είναι ένας σαφέστερος τρόπος να το σκεφτείτε:
* ομοιοπολικά ομόλογα Προσδιορίστε τη δομή ενός μορίου .
* Διαμοριακές δυνάμεις Προσδιορίστε την κατάσταση της ύλης (στερεό, υγρό ή αέριο).
Έτσι, ενώ οι ομοιοπολικοί δεσμοί εξακολουθούν να υπάρχουν σε υγρά, είναι οι ασθενέστερες ενδομοριακές δυνάμεις που επιτρέπουν στα μόρια να κινούνται πιο ελεύθερα.