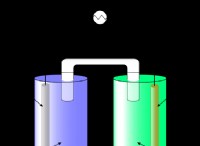
Τι δείχνουν οι μισές αντιδράσεις;
Τι δείχνουν:
* Μεταφορά ηλεκτρονίων: Παρουσιάζουν σαφώς την κίνηση των ηλεκτρονίων κατά τη διάρκεια της αντίδρασης.
* Οξείδωση ή μείωση: Οι μισές αντιδράσεις προσδιορίζουν ποια είδη οξειδώνονται (απώλεια ηλεκτρονίων) και τα οποία μειώνονται (κερδίζοντας ηλεκτρόνια).
* εξισορρόπηση ατόμων και χρεώσεων: Οι μισές αντιδράσεις είναι ισορροπημένες για να εξασφαλίσουν ότι ο αριθμός των ατόμων και των χρεώσεων είναι ο ίδιος και από τις δύο πλευρές.
Παράδειγμα:
Ας εξετάσουμε την αντίδραση μεταξύ ιόντων μεταλλικού ψευδαργύρου και χαλκού (II):
Συνολική αντίδραση: Zn (s) + Cu²⁺ (aq) → Zn²⁺ (aq) + cu (s)
μισή αντίδραση:
* Οξείδωση: Zn (s) → Zn²⁺ (aq) + 2e⁻
* Μείωση: Cu²⁺ (aq) + 2e⁻ → cu (s)
Επεξήγηση:
* Η μισή αντίδραση οξείδωσης δείχνει ότι ο ψευδάργυρος χάνει δύο ηλεκτρόνια για να γίνει ιόν ψευδαργύρου (zn²⁺).
* Η μείωση της μείωσης της μείωσης Δείχνει ιόντα χαλκού που κερδίζουν δύο ηλεκτρόνια για να γίνουν μεταλλικοί χαλκός.
Γιατί είναι σημαντικά;
* Κατανόηση αντιδράσεων οξειδοαναγωγής: Μας βοηθούν να κατανοήσουμε τις θεμελιώδεις διαδικασίες που εμπλέκονται σε αντιδράσεις οξειδοαναγωγής.
* Πρόβλεψη σκοπιμότητας αντίδρασης: Αναλύοντας τις μισές αντιδράσεις, μπορούμε να διαπιστώσουμε εάν μια αντίδραση θα συμβεί αυθόρμητα ή όχι.
* Εξισορρόπηση σύνθετων οξειδοαναγωγικών αντιδράσεων: Η εξισορρόπηση των μισών αντιδράσεων καθιστά την εξισορρόπηση της συνολικής αντίδρασης οξειδοαναγωγής πολύ πιο εύκολη.
Βασικά σημεία:
* Κάθε μισή αντίδραση περιλαμβάνει μόνο οξείδωση ή μείωση, όχι και τα δύο.
* Τα ηλεκτρόνια παρουσιάζονται ως προϊόντα σε αντιδράσεις οξείδωσης και αντιδραστήρια σε αντιδράσεις μείωσης.
* Ο αριθμός των ηλεκτρονίων που χάνονται στην οξείδωση μισή αντίδραση πρέπει να ισούται με τον αριθμό των ηλεκτρονίων που αποκτήθηκαν στη μείωση της μισής αντίδρασης.
Οι μισές αντιδράσεις παρέχουν ένα απλοποιημένο και ισχυρό εργαλείο για την κατανόηση και την ανάλυση του σύνθετου κόσμου της χημείας οξειδοαναγωγής.