Πώς μπορείτε να πείτε εάν ένα καθαρό υγρό είναι καθαρό ή ήταν μείγμα;
Γιατί είναι δύσκολο:
* Πολλά μείγματα εμφανίζονται καθαρά: Η ζάχαρη διαλύεται σε νερό, το αλάτι που διαλύεται σε νερό και ακόμη και ο αέρας (ένα μείγμα αερίων) φαίνεται καθαρό.
* Οι καθαρές ουσίες μπορεί να είναι σαφείς: Το νερό, το αλκοόλ και πολλά άλλα καθαρά υγρά είναι διαφανή.
Πώς να προσπαθήσετε να το καταλάβετε:
1. σημείο βρασμού: Οι καθαρές ουσίες έχουν ένα συγκεκριμένο, σταθερό σημείο βρασμού. Ένα μείγμα θα έχει μια σειρά σημείων βρασμού. Εάν το υγρό βράζει σε σταθερή θερμοκρασία, είναι πιο πιθανό να είναι καθαρό.
2. Σημείο κατάψυξης: Παρόμοια με το σημείο βρασμού, οι καθαρές ουσίες έχουν ένα συγκεκριμένο σημείο κατάψυξης. Τα μείγματα παγώνουν σε μια σειρά θερμοκρασιών.
3. Πυκνότητα: Κάθε καθαρή ουσία έχει μια μοναδική πυκνότητα. Μπορείτε να μετρήσετε την πυκνότητα του υγρού και να το συγκρίνετε με γνωστές πυκνότητες καθαρών ουσιών.
4. Γεύση και μυρωδιά: Ορισμένες ουσίες έχουν διακριτικές προτιμήσεις ή μυρωδιές που μπορούν να σας βοηθήσουν να τα εντοπίσετε. Ωστόσο, αυτό δεν είναι ένα αξιόπιστο επιστημονικό τεστ.
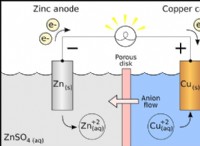
5. Το καθαρό νερό είναι ένας κακός αγωγός ηλεκτρικής ενέργειας, ενώ τα διαλύματα που περιέχουν διαλυμένα άλατα ή οξέα θα διεξάγουν ηλεκτρική ενέργεια.
6. Ποσοστό εξάτμισης: Ορισμένα υγρά εξατμίζονται ταχύτερα από άλλα. Εάν το υγρό εξατμίζεται πολύ γρήγορα, μπορεί να είναι μια πτητική ουσία.
7. φασματοσκοπία: Αυτή η εξελιγμένη τεχνική χρησιμοποιεί φως για να αναλύσει τη χημική μακιγιάζ μιας ουσίας. Μπορεί να προσδιορίσει οριστικά εάν μια ουσία είναι καθαρή ή μείγμα.
Σημαντική σημείωση:
* Ασφάλεια πρώτα: Ποτέ μην δοκιμάζετε ή μυρίζετε ένα άγνωστο υγρό. Ορισμένες ουσίες μπορεί να είναι επικίνδυνες!
* Πειραματισμός: Για να προσδιορίσετε πραγματικά εάν ένα καθαρό υγρό είναι καθαρό ή μείγμα, θα πρέπει να εκτελέσετε δοκιμές και πειράματα.
Επιτρέψτε μου να ξέρω αν θέλετε να εξερευνήσετε κάποια από αυτές τις μεθόδους με περισσότερες λεπτομέρειες!