Ποιες μεταβολές του ρΗ συμβαίνουν όταν οι αντιδράσεις εξουδετέρωσης μεταξύ δύο ονομασμένων οξέων και μιας βάσης;
Μεταβολές του ρΗ στις αντιδράσεις εξουδετέρωσης
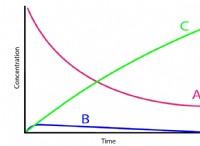
Οι αντιδράσεις εξουδετέρωσης περιλαμβάνουν την αντίδραση μεταξύ ενός οξέος και μιας βάσης, με αποτέλεσμα τον σχηματισμό αλατιού και νερού. Αυτή η αντίδραση οδηγεί σε σημαντικές μεταβολές του ρΗ, καθώς εξουδετερώνονται οι όξινες και βασικές ιδιότητες των αντιδραστηρίων.
Ακολουθεί μια ανάλυση των αλλαγών του ρΗ κατά τη διάρκεια των αντιδράσεων εξουδετέρωσης με δύο ονομασμένα οξέα και μια βάση:
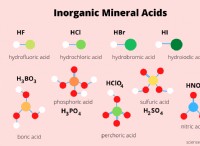
1. Υδροχλωρικό οξύ (HCl) και υδροξείδιο του νατρίου (ΝαΟΗ)
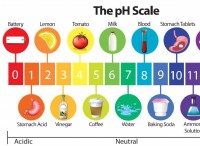
* hcl: Ένα ισχυρό οξύ, που σημαίνει ότι εντελώς ιονίζει στο νερό, απελευθερώνοντας ιόντα Η+, οδηγώντας σε χαμηλό ρΗ (συνήθως γύρω στο 0-1).
* naoh: Μια ισχυρή βάση, που σημαίνει ότι είναι πλήρως ιονίζει στο νερό, απελευθερώνοντας ιόντα, οδηγώντας σε υψηλό ρΗ (συνήθως περίπου 13-14).
αντίδραση: HCl + NaOH → NaCl + H2O
αλλαγή pH: Η αντίδραση έχει ως αποτέλεσμα το σχηματισμό άλατος (NaCl), το οποίο είναι ουδέτερο και νερό (H2O), το οποίο είναι επίσης ουδέτερο. Αυτή η εξουδετέρωση οδηγεί σε μείωση του ρΗ για το HCl και αύξηση του pH για NaOH , τελικά φτάνοντας σε ένα ουδέτερο pH του 7.
2. Οξετικό οξύ (CH3COOH) και υδροξείδιο του καλίου (KOH)
* CH3COOH: Ένα αδύναμο οξύ, που σημαίνει ότι μόνο εν μέρει ιονίζει στο νερό, απελευθερώνοντας λιγότερα ιόντα Η+ σε σύγκριση με ισχυρά οξέα, οδηγώντας σε υψηλότερο ρΗ (συνήθως περίπου 2-3) από το HCl.
* koh: Μια ισχυρή βάση, που σημαίνει ότι είναι πλήρως ιονίζει στο νερό, απελευθερώνοντας ιόντα, οδηγώντας σε υψηλό ρΗ (συνήθως περίπου 13-14).
αντίδραση: CH3COOH + KOH → CH3COOK + H2O
αλλαγή pH: Η αντίδραση σχηματίζει οξικό κάλιο (CH3COOK), αλάτι και νερό. Αυτή η εξουδετέρωση οδηγεί επίσης σε μείωση του ρΗ για το CH3COOH και την αύξηση του pH για το KOH , αλλά το τελικό pH θα είναι ελαφρώς υψηλότερο από 7 λόγω της αδύναμης φύσης του οξικού οξέος.
Γενικές παρατηρήσεις:
* Ισχυρό οξύ + ισχυρή βάση: Η εξουδετέρωση έχει ως αποτέλεσμα ένα ουδέτερο ρΗ 7.
* Αδύναμο οξύ + Ισχυρή βάση: Η εξουδετέρωση έχει ως αποτέλεσμα ένα ελαφρώς βασικό pH (πάνω από 7).
* Ισχυρό οξύ + Αδύναμη βάση: Η εξουδετέρωση έχει ως αποτέλεσμα ένα ελαφρώς όξινο ρΗ (κάτω από 7).
Συμπέρασμα:
Οι αντιδράσεις εξουδετέρωσης περιλαμβάνουν την εξουδετέρωση των όξινων και βασικών ιδιοτήτων, οδηγώντας σε σημαντικές μεταβολές στο pH. Το τελικό ρΗ εξαρτάται από την αντοχή του οξέος και της βάσης, με ισχυρά οξέα και βάσεις με αποτέλεσμα το ουδέτερο ρΗ, ενώ τα αδύναμα οξέα ή οι βάσεις οδηγούν σε ελαφρώς όξινα ή βασικά διαλύματα.