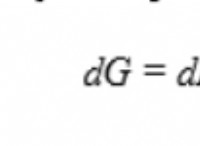Γιατί το PENT-1-OL βράζει στο 137Degree Centigrade ενώ το Pent-3-OL 116 βαθμού Centigrade;
Εδώ είναι γιατί:
* pent-1-ol (πρωτογενές αλκοόλ): Η ομάδα υδροξυλίου (ΟΗ) σε PENT-1-OL συνδέεται με έναν άνθρακα που συνδέεται άμεσα μόνο σε ένα άλλο άτομο άνθρακα. Αυτό καθιστά το υδρογόνο στην ομάδα υδροξυλίου πιο όξινο και επομένως πιο επιρρεπές στη δέσμευση υδρογόνου.
* Pent-3-Ol (δευτερεύουσα αλκοόλη): Η ομάδα υδροξυλίου σε Pent-3-OL συνδέεται με έναν άνθρακα που συνδέεται άμεσα με δύο άλλα άτομα άνθρακα. Αυτό καθιστά το υδρογόνο στην ομάδα υδροξυλίου λιγότερο όξινο σε σύγκριση με το PENT-1-OL, οδηγώντας σε ασθενέστερη δέσμευση υδρογόνου.
Η σύνδεση υδρογόνου είναι μια ισχυρή διαμοριακή δύναμη που απαιτεί σημαντική ενέργεια για να ξεπεραστεί. Δεδομένου ότι το PENT-1-OL σχηματίζει ισχυρότερους δεσμούς υδρογόνου από το Pent-3-OL, απαιτεί περισσότερη ενέργεια για να σπάσει αυτούς τους δεσμούς και να εξατμιστεί, με αποτέλεσμα ένα υψηλότερο σημείο βρασμού.
Συνοπτικά:
* Η ισχυρότερη δέσμευση υδρογόνου σε Pent-1-OL οδηγεί σε υψηλότερο σημείο βρασμού σε σύγκριση με το Pent-3-Ol
* Η θέση της ομάδας υδροξυλίου επηρεάζει τη δύναμη της σύνδεσης υδρογόνου και επομένως το σημείο βρασμού