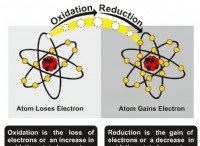
Τι συμβαίνει στη διαδικασία της ιοντικής σύνδεσης;
Ακολουθεί μια ανάλυση της διαδικασίας:
1. Μεταφορά ηλεκτρονίων: Ένα άτομο, συνήθως ένα μέταλλο, θα χάσει ένα ή περισσότερα ηλεκτρόνια από το εξωτερικό του κέλυφος. Αυτό το άτομο γίνεται Cation , ένα θετικά φορτισμένο ιόν. Το άλλο άτομο, συνήθως ένα μέταλλο, θα κερδίσει αυτά τα ηλεκτρόνια, θα γίνει ανιόν , ένα αρνητικά φορτισμένο ιόν.
2. Ηλεκτροστατική έλξη: Λόγω των αντίθετων φορτίων τους, το κατιόν και το ανιόν προσελκύονται έντονα μεταξύ τους μέσω ηλεκτροστατικών δυνάμεων. Αυτό το αξιοθέατο σχηματίζει τον ιονικό δεσμό.
3. σχηματισμός ιοντικής ένωσης: Τα αντίθετα φορτισμένα ιόντα οργανώνονται σε ένα κανονικό, επαναλαμβανόμενο μοτίβο που ονομάζεται κρυσταλλικό πλέγμα . Αυτή η δομή πλέγματος συγκρατείται από τις ισχυρές ηλεκτροστατικές δυνάμεις μεταξύ των ιόντων.
Παράδειγμα:
* νάτριο (Na) και χλώριο (CL): Το νάτριο έχει ένα ηλεκτρόνιο σθένους, ενώ το χλώριο χρειάζεται ένα ηλεκτρόνιο για να ολοκληρώσει το εξωτερικό του κέλυφος.
* Το νάτριο χάνει το ηλεκτρόνιο του να γίνει θετικά φορτισμένο ιόν νατρίου (Na+).
* Χλωρίνη κερδίζει αυτό το ηλεκτρόνιο να γίνει ένα αρνητικά φορτισμένο χλωριούχο ιόν (cl-).
* Τα Na+ και Cl-ions προσελκύουν το ένα το άλλο σχηματίζοντας δομή κρυσταλλικού πλέγματος, με αποτέλεσμα το χλωριούχο νάτριο ιοντικής ένωσης (NaCl) ή το αλάτι επιτραπέζιου.
Βασικά χαρακτηριστικά της ιοντικής σύνδεσης:
* υψηλά σημεία τήξης και βρασμού: Λόγω ισχυρών ηλεκτροστατικών αξιοθέατων.
* σκληρό και εύθραυστο: Η δομή του άκαμπτου κρυσταλλικού πλέγματος διαταράσσεται εύκολα με δύναμη.
* καλοί αγωγοί ηλεκτρικής ενέργειας όταν διαλύονται σε νερό ή λιωμένο: Τα ιόντα ελεύθερης κίνησης μπορούν να μεταφέρουν ηλεκτρικό ρεύμα.
* Συνήθως σχηματίζεται μεταξύ μετάλλων και μη μετάλλων: Τα μέταλλα τείνουν να χάνουν ηλεκτρόνια, ενώ τα μη μέταλλα τείνουν να κερδίζουν ηλεκτρόνια.
Συνολικά, η ιοντική σύνδεση είναι μια θεμελιώδης διαδικασία στη χημεία που οδηγεί στο σχηματισμό μιας ευρείας ποικιλίας σημαντικών ενώσεων με μοναδικές ιδιότητες.