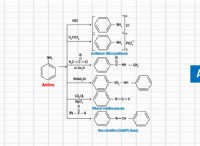
Είναι μια οργανική ένωση δακτυλίου που συχνά φαίνεται να έχει εναλλασσόμενες μονές και διπλές δεσμούς, όλα αυτά έχουν τις ίδιες ενέργειες δεσμών;
Παρόλο που συχνά σχεδιάζεται με εναλλασσόμενους μεμονωμένους και διπλούς δεσμούς, η πραγματικότητα είναι πιο λεπτή:
* Οι ενέργειες των ομολόγων είναι ίσες: Τα ομόλογα σε αρωματικούς δακτυλίους είναι όχι Πραγματικά ενιαίοι ή διπλοί δεσμοί. Είναι όλα ισοδύναμα και έχουν μια σειρά ομολόγων 1,5, η οποία είναι ενδιάμεση μεταξύ ενός και ενός διπλού δεσμού. Αυτό οφείλεται στη μετεγκατάσταση των ηλεκτρονίων σε όλο το δακτύλιο, δημιουργώντας ένα "σύννεφο" πυκνότητας ηλεκτρονίων.
* Delocalization: Τα ηλεκτρόνια στο δακτύλιο δεν εντοπίζονται μεταξύ συγκεκριμένων ατόμων, αλλά μάλλον απλωμένα σε ολόκληρο το σύστημα δακτυλίων. Αυτή η απομάκρυνση είναι αυτό που καθιστά τις αρωματικές ενώσεις ιδιαίτερα σταθερές και αντιδραστικές.
Έτσι, ενώ η εκπροσώπηση με εναλλασσόμενους μεμονωμένους και διπλούς δεσμούς είναι ένας βολικός τρόπος για την απεικόνιση της αρωματικότητας, είναι σημαντικό να θυμόμαστε ότι όλοι οι δεσμοί σε ένα αρωματικό δακτύλιο είναι στην πραγματικότητα ισοδύναμες και έχουν μια σειρά δεσμού 1,5.