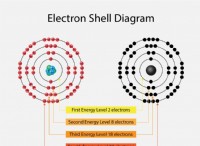
Τι μπορεί να σχηματίσει ένα ιοντικό δεσμό;
* μέταλλα τείνουν να χάνουν ηλεκτρόνια, σχηματίζοντας θετικά φορτισμένα ιόντα που ονομάζονται κατιόντα .
* Μη μέταλλα τείνουν να κερδίζουν ηλεκτρόνια, σχηματίζοντας αρνητικά φορτισμένα ιόντα που ονομάζονται anions .
Η ισχυρή ηλεκτροστατική έλξη μεταξύ αυτών των αντίθετα φορτισμένων ιόντων είναι αυτό που δημιουργεί τον ιοντικό δεσμό.
Εδώ είναι ένα απλό παράδειγμα:
* νάτριο (na) , ένα μέταλλο, χάνει ένα ηλεκτρόνιο για να γίνει ένα ιόν νατρίου (Na+).
* χλώριο (cl) , ένα μη μέταλλο, κερδίζει ένα ηλεκτρόνιο για να γίνει ένα χλωριούχο ιόν (cl-).
* Αυτά τα αντίθετα φορτισμένα ιόντα στη συνέχεια προσελκύουν ο ένας τον άλλον, σχηματίζοντας χλωριούχο νάτριο (NaCl), επίσης γνωστό ως επιτραπέζιο αλάτι.
Βασικοί παράγοντες για τον σχηματισμό ιοντικών δεσμών:
* Διαφορά ηλεκτροαρνητικότητας: Μια σημαντική διαφορά ηλεκτροαρνητικότητας μεταξύ των δύο ατόμων είναι απαραίτητη για ένα άτομο να μεταφέρει πλήρως ένα ηλεκτρόνιο στο άλλο.
* ενέργεια ιονισμού: Η ενέργεια που απαιτείται για την απομάκρυνση ενός ηλεκτρονίου από ένα άτομο πρέπει να είναι σχετικά χαμηλή για το μέταλλο.
* συγγένεια ηλεκτρονίων: Η αλλαγή ενέργειας όταν ένα άτομο κερδίζει ένα ηλεκτρόνιο πρέπει να είναι ευνοϊκή για το μη μέταλλο.
Συνοπτικά, οι ιοντικοί δεσμοί σχηματίζονται από την ηλεκτροστατική έλξη μεταξύ αντίθετα φορτισμένων ιόντων, τα οποία δημιουργούνται με τη μεταφορά ηλεκτρονίων μεταξύ ενός μετάλλου και ενός μη μεταλλικού.