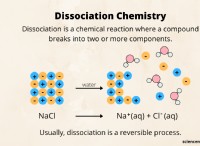
Ποια είναι η διαδικασία στην οποία τα μόρια σπάζουν από τον εθισμό των μορίων νερού;
Δείτε πώς λειτουργεί:
* Το νερό (h₂o) είναι ένα πολικό μόριο , που σημαίνει ότι έχει ένα ελαφρώς θετικό τέλος και ένα ελαφρώς αρνητικό τέλος.
* Αυτή η πολικότητα επιτρέπει στο νερό να αλληλεπιδρά με και να χωρίζει άλλα πολικά μόρια.
* Στην υδρόλυση, το μόριο νερού διασπάται σε ένα ιόν υδρογόνου (H⁺) και ένα ιόν υδροξειδίου (OH⁻) .
* Αυτά τα ιόντα στη συνέχεια συνδέονται με το μόριο που διασπώνται, εξασθενίζοντας τους δεσμούς που το συγκρατούν μαζί.
* Αυτό έχει ως αποτέλεσμα το μόριο να χωρίζεται σε δύο ή περισσότερα μικρότερα μόρια .
Παραδείγματα υδρόλυσης:
* πέψη: Η υδρόλυση είναι απαραίτητη για τη διάσπαση των μορίων τροφίμων όπως οι υδατάνθρακες, οι πρωτεΐνες και τα λίπη σε μικρότερες μονάδες που μπορούν να απορροφηθούν από το σώμα.
* ΔΙΑΚΟΠΗ ΑΤΡ: Το ενεργειακό νόμισμα των κυττάρων, ΑΤΡ, διασπάται με υδρόλυση για την απελευθέρωση ενέργειας για κυτταρικές διεργασίες.
* Καταστροφή πολυμερούς: Τα πολυμερή όπως το άμυλο και η κυτταρίνη χωρίζονται σε μικρότερα μονομερή με υδρόλυση.
Συνοπτικά , η υδρόλυση είναι μια κρίσιμη διαδικασία για τη διάσπαση των μεγάλων μορίων σε μικρότερα, επιτρέποντας μια ποικιλία βασικών βιολογικών και χημικών αντιδράσεων.