Ποια είναι η συγκέντρωση οξικού οξέος και ρΗ σε ένα διάλυμα που ιονισμένο 0,25;
Κατανόηση των εννοιών
* οξικό οξύ (ch₃cooh): Ένα αδύναμο οξύ που μόνο εν μέρει ιονίζει στο νερό.
* ιονισμός: Η διαδικασία όπου ένα οξύ απελευθερώνει ένα πρωτόνιο (H⁺) σε διάλυμα.
* Ισορροπία: Η κατάσταση όπου ο ρυθμός ιονισμού και ο ρυθμός ανασυνδυασμού των ιόντων είναι ίσοι.
* ka (σταθερά διάστασης οξέος): Ένα μέτρο της αντοχής ενός οξέος. Μια χαμηλότερη τιμή ΚΑ υποδεικνύει ένα ασθενέστερο οξύ. Για οξικό οξύ, ΚΑ =1,8 x 10⁻⁵.
Υπολογισμοί
1. Αρχική συγκέντρωση: Πρέπει να γνωρίζουμε την αρχική συγκέντρωση του διαλύματος οξικού οξέος (ας το ονομάσουμε "C") για να προχωρήσουμε με τους υπολογισμούς.
2. συγκεντρώσεις ισορροπίας:
* [ch₃cooh]: Η συγκέντρωση του μη κινητικού οξικού οξέος σε ισορροπία είναι (1 - 0,25) C =0,75C
* [ch₃coo⁻]: Η συγκέντρωση ιόντων οξικών σε ισορροπία είναι 0,25C
* [h⁺]: Η συγκέντρωση ιόντων υδρογόνου σε ισορροπία είναι επίσης 0,25C (επειδή κάθε μόριο οξικού οξέος που ιονίζει απελευθερώνει ένα ιόν H⁺)
3. Έκφραση ka:
Ka =[ch₃coo⁻] [h⁺] / [ch₃cooh]
1,8 x 10⁻⁵ =(0,25C) (0,25C) / 0,75C
1,8 x 10⁻⁵ =0,0833c
C =2,16 x 10⁻⁴ m (αυτή είναι η αρχική συγκέντρωση οξικού οξέος)
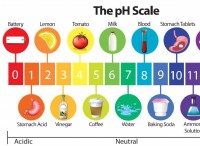
4. ph:
ph =-log [h⁺]
ph =-log (0.25 * 2.16 x 10⁻⁴)
ph =3,67
Περίληψη:
* Συγκέντρωση οξικού οξέος: 2.16 x 10⁻⁴ m
* ph: 3.67
Σημαντική σημείωση: Το ποσοστό ιονισμού του οξικού οξέος δεν είναι σταθερή τιμή. Εξαρτάται από την αρχική συγκέντρωση του οξέος.