Μπορεί το αέριο να χωριστεί σε απλούστερες ουσίες;
Εδώ είναι μια κατανομή:
1. Εάν μιλάτε για ένα καθαρό στοιχείο στην αέρια του κατάσταση (όπως το οξυγόνο, το άζωτο ή το υδρογόνο):
* Όχι, αυτά δεν μπορούν να αναλυθούν σε απλούστερες ουσίες. Είναι ήδη οι απλούστερες μορφές ύλης.
2. Εάν μιλάτε για μια ένωση στην αέρια του κατάσταση (όπως το διοξείδιο του άνθρακα, το μεθάνιο ή η αμμωνία):
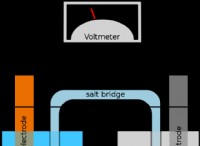
* Ναι, αυτά μπορούν να χωριστούν σε απλούστερες ουσίες. Αποτελούνται από δύο ή περισσότερα στοιχεία που συνδέονται χημικά μαζί. Η διάσπαση αυτών των δεσμών μέσω χημικών αντιδράσεων μπορεί να διαχωρίσει την ένωση στα συστατικά της. Για παράδειγμα, μέσω της ηλεκτρόλυσης, το νερό (H₂O) μπορεί να χωριστεί σε υδρογόνο (H₂) και οξυγόνο (O₂).
3. Εάν μιλάτε για ένα μείγμα αερίων:
* Όχι, αυτά δεν μπορούν να αναλυθούν σε απλούστερες ουσίες, αλλά μπορούν να διαχωριστούν. Ένα μείγμα είναι ένας συνδυασμός ουσιών που δεν είναι χημικά συνδεδεμένες. Μπορούν να διαχωριστούν με φυσικά μέσα, όπως απόσταξη ή διήθηση, για να απομονώσουν τα μεμονωμένα συστατικά.
Έτσι, για να απαντήσετε στην ερώτησή σας συνοπτικά:
* Τα αέρια καθαρού στοιχείου δεν μπορούν να χωριστούν σε απλούστερες ουσίες.
* Τα σύνθετα αέρια μπορούν να διασπαστούν σε απλούστερες ουσίες μέσω χημικών αντιδράσεων.
* Μείγματα αερίων μπορούν να διαχωριστούν με φυσικά μέσα.
Επιτρέψτε μου να ξέρω αν έχετε περισσότερες ερωτήσεις!