Τι κάνουν τα μόρια σε ένα στερεό συγκράτηση;
Ακολουθεί μια κατανομή των κύριων τύπων διαμοριακών δυνάμεων:
* Van der Waals Δυνάμεις: Αυτές είναι αδύναμες, προσωρινές δυνάμεις που προκύπτουν από προσωρινές διακυμάνσεις στην κατανομή ηλεκτρονίων γύρω από τα μόρια. Χωρίζονται περαιτέρω σε:
* Δυνάμεις διασποράς του Λονδίνου: Αυτοί είναι ο πιο αδύναμος τύπος δυνάμεων van der Waals, που υπάρχουν σε όλα τα μόρια.
* Δυνάμεις διπόλης: Αυτά συμβαίνουν μεταξύ πολικών μορίων που έχουν μόνιμο διαχωρισμό του φορτίου.
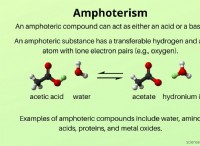
* δεσμός υδρογόνου: Ένας ειδικός τύπος δύναμης διπολικού-δίπολου όπου το υδρογόνο συνδέεται με ένα εξαιρετικά ηλεκτροαρνητικό άτομο όπως το οξυγόνο, το άζωτο ή το φθορίνη. Είναι ο ισχυρότερος τύπος διαμοριακής δύναμης.
* Ιονικές δυνάμεις: Αυτά είναι ισχυρά ηλεκτροστατικά αξιοθέατα μεταξύ των αντιθέτων ιόντων. Εμφανίζονται σε ιοντικές ενώσεις όπου μεταφέρονται ηλεκτρόνια μεταξύ των ατόμων.
Ο τύπος της διαμοριακής δύναμης που υπάρχει σε ένα στερεό καθορίζει τις ιδιότητές του όπως το σημείο τήξης, το σημείο βρασμού και τη σκληρότητα. Για παράδειγμα, τα στερεά με ισχυρή δέσμευση υδρογόνου τείνουν να έχουν υψηλά σημεία τήξης, ενώ τα στερεά με αδύναμες δυνάμεις van der Waals έχουν χαμηλά σημεία τήξης.