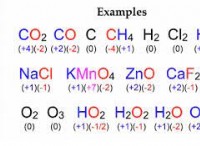
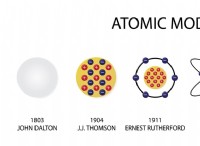
Ποιες είναι οι ιδιότητες του σιδήρου και του άνθρακα;
Ιδιότητες του σιδήρου (Fe)
Φυσικές ιδιότητες:
* εμφάνιση: Ασημί-γκρι, λαμπερό, εύπλαστο, όλκιμο
* Πυκνότητα: 7.874 g/cm3
* Σημείο τήξης: 1538 ° C (2800 ° F)
* σημείο βρασμού: 2862 ° C (5184 ° F)
* σκληρότητα: Ποικίλλει ανάλογα με τη φόρμα (ο καθαρός σίδηρος είναι μαλακός, ο χάλυβας είναι σκληρός)
* Μαγνητικές ιδιότητες: Σιδηρομαγνητικό (έντονα προσελκύεται από μαγνήτες)
* Ηλεκτρική αγωγιμότητα: Καλός αγωγός ηλεκτρικής ενέργειας
* Θερμική αγωγιμότητα: Καλός αγωγός θερμότητας
Χημικές ιδιότητες:
* Αντιδραστικότητα: Αντιδρά με οξυγόνο για να σχηματίσει οξείδιο του σιδήρου (σκουριά)
* καταστάσεις οξείδωσης: Οι κοινές καταστάσεις οξείδωσης είναι +2 και +3
* σχηματίζει ενώσεις: Σχηματίζει διάφορες ενώσεις με άλλα στοιχεία, συμπεριλαμβανομένων των οξειδίων, των χλωριδίων, των σουλφιδίων και των ανθρακικών αλάτων.
key χρησιμοποιεί:
* Κατασκευή: Οικοδομικά υλικά, γέφυρες, οχήματα
* Κατασκευή: Παραγωγή χάλυβα, μηχανήματα, εργαλεία
* Ηλεκτρονικά: Μαγνητικά υλικά, ηλεκτρικά εξαρτήματα
* φάρμακο: Συμπληρώματα σιδήρου, ιατρικές συσκευές
Ιδιότητες του άνθρακα (c)
Φυσικές ιδιότητες:
* εμφάνιση: Ποικίλλει ανάλογα με το αλλοτρόπο (το διαμάντι είναι διαφανές, ο γραφίτης είναι μαύρος)
* Πυκνότητα: Ποικίλλει ανάλογα με το αλλοτρόπο (το διαμάντι είναι 3,51 g/cm³, ο γραφίτης είναι 2,267 g/cm3)
* Σημείο τήξης: Ποικίλλει ανάλογα με το αλλοτρόπο (το διαμάντι είναι 4000 ° C, ο γραφίτης είναι 3550 ° C)
* σημείο βρασμού: Υποεπιτροπές στους 4827 ° C
* σκληρότητα: Ποικίλλει ανάλογα με το αλλοτρόπο (το διαμάντι είναι το πιο δύσκολο φυσικό υλικό, ο γραφίτης είναι μαλακός)
* Ηλεκτρική αγωγιμότητα: Ποικίλλει ανάλογα με το αλλοτρόπο (το Diamond είναι ένας μονωτήρας, ο γραφίτης είναι αγωγός)
* Θερμική αγωγιμότητα: Ποικίλλει ανάλογα με το allotrope (το Diamond είναι καλός αγωγός, ο γραφίτης είναι ένας κακός αγωγός)
Χημικές ιδιότητες:
* Αντιδραστικότητα: Αντιδρά με οξυγόνο για να σχηματίσει διοξείδιο του άνθρακα (CO2), αλλά σχηματίζει και άλλες ενώσεις όπως το μονοξείδιο του άνθρακα (CO)
* καταστάσεις οξείδωσης: Κυμαίνεται από -4 έως +4
* σχηματίζει ενώσεις: Σχηματίζει πολυάριθμες ενώσεις, συμπεριλαμβανομένων οργανικών ενώσεων, ανθρακικών και καρβίδων
key χρησιμοποιεί:
* καύσιμο: Άνθρακας, φυσικό αέριο, πετρέλαιο
* Υλικά: Diamond (κοσμήματα, εργαλεία κοπής), γραφίτη (μολύβια, λιπαντικά)
* Χημεία: Βάση για οργανική χημεία, δομικό στοιχείο για πολλές ενώσεις
* Ηλεκτρονικά: Υλικά ημιαγωγών
Σημαντική σημείωση: Τόσο ο σίδηρος όσο και ο άνθρακας υπάρχουν σε διάφορες μορφές που ονομάζονται αλλοτροπές. Οι αλλοτροπές έχουν διαφορετικές φυσικές και χημικές ιδιότητες. Για παράδειγμα, το Diamond και ο γραφίτης είναι και οι δύο αλλοτροπές άνθρακα.
Αυτή είναι μια απλοποιημένη επισκόπηση των ιδιοτήτων του σιδήρου και του άνθρακα. Και τα δύο στοιχεία έχουν ένα ευρύ φάσμα ιδιοτήτων και είναι ζωτικής σημασίας σε πολλούς τομείς της επιστήμης και της τεχνολογίας.