Ποιος είναι ο σύνδεσμος μεταξύ της ομάδας ένα μέταλλο και της φόρτισης στο ιόν του;
Ομάδα 1 μέταλλα σχηματίζουν πάντα +1 ιόντα
Εδώ είναι γιατί:
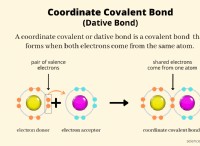
* Διαμόρφωση ηλεκτρονίων: Τα αλκαλικά μέταλλα έχουν ένα ηλεκτρόνιο σθένους στο εξωτερικό κέλυφος τους. Αυτό το ηλεκτρόνιο χάνεται εύκολα για να επιτευχθεί μια σταθερή διαμόρφωση ηλεκτρονίων όπως τα ευγενή αέρια.
* Ηλεκτροποσωτικότητα: Τα αλκαλικά μέταλλα είναι εξαιρετικά ηλεκτριστικά, πράγμα που σημαίνει ότι έχουν έντονη τάση να χάσουν ηλεκτρόνια.
* Ιονική σύνδεση: Όταν τα αλκαλικά μέταλλα αντιδρούν με μη μέταλλα, χάνουν αυτό το ηλεκτρόνιο σθένους για να σχηματίσουν ένα θετικά φορτισμένο ιόν με φορτίο +1.
Παραδείγματα:
* λίθιο (li) μορφές li+
* νάτριο (na) Φόρμα Na+
* κάλιο (k) σχηματίζει k+
* rubidium (RB) Έντυπα RB+
* Cesium (CS) Έντυπα CS+
Αυτό το συνεπές +1 φορτίο για όλα τα μέταλλα της ομάδας 1 τους καθιστά προβλέψιμες και σχετικά εύκολο να εργαστούν σε χημικές αντιδράσεις.