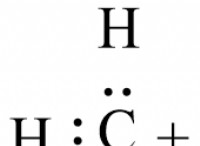Πώς ο δεσμός άνθρακα με οξυγόνο;
* Ηλεκτροργατιστικότητα: Το οξυγόνο είναι πιο ηλεκτροαρνητικό από τον άνθρακα, που σημαίνει ότι έχει ισχυρότερη έλξη σε κοινόχρηστα ηλεκτρόνια.
* Κοινή χρήση ηλεκτρόνων: Ο άνθρακας έχει τέσσερα ηλεκτρόνια σθένους και το οξυγόνο έχει έξι. Για να επιτύχουν ένα σταθερό οκτάδα (οκτώ ηλεκτρόνια στο εξωτερικό τους κέλυφος), μοιράζονται ηλεκτρόνια.
* Διπλός δεσμός: Σε έναν κοινό δεσμό άνθρακα-οξυγόνου (όπως στο διοξείδιο του άνθρακα, CO2), ο άνθρακας μοιράζεται δύο από τα ηλεκτρόνια του με κάθε άτομο οξυγόνου, δημιουργώντας διπλό δεσμό. Αυτός ο δεσμός είναι ισχυρός και σταθερός.
Εδώ είναι μερικά βασικά σημεία για να θυμάστε:
* πολικότητα: Η άνιση κατανομή των ηλεκτρονίων σε έναν δεσμό άνθρακα-οξυγόνου δημιουργεί έναν πολικό ομοιοπολικό δεσμό, όπου το άτομο οξυγόνου έχει ελαφρώς αρνητικό φορτίο και το άτομο άνθρακα έχει ελαφρώς θετικό φορτίο.
* Πολλαπλά ομόλογα: Ο άνθρακας μπορεί να σχηματίσει μεμονωμένους, διπλούς ή τριπλούς δεσμούς με οξυγόνο, ανάλογα με το μόριο.
* Σημασία στη βιολογία: Ο δεσμός μεταξύ άνθρακα και οξυγόνου είναι ζωτικής σημασίας για τη ζωή όπως τον γνωρίζουμε. Σχηματίζει τη σπονδυλική στήλη βασικών μορίων όπως υδατάνθρακες, λιπίδια και πρωτεΐνες.
Επιτρέψτε μου να ξέρω αν θέλετε μια πιο εμπεριστατωμένη εξήγηση συγκεκριμένων παραδειγμάτων όπως το διοξείδιο του άνθρακα ή αν θέλετε να μάθετε περισσότερα για την πολικότητα του δεσμού!