Δώστε μια εξήγηση για τη σειρά της αντιδραστικότητας που παρατηρούνται τρία κορεσμένα αλκυλαλογονίδια με Ag Plus;
Η αντίδραση:
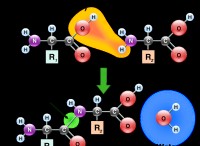
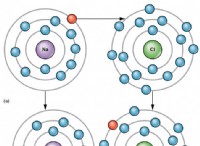
Η αντίδραση μεταξύ κορεσμένων αλκυλαλογονιδίων και ιόντων αργύρου είναι μια αντίδραση πυρηνόφιλης υποκατάστασης . Το ασημένιο ιόν ενεργεί ως Lewis Acid , αποδοχή ενός ζεύγους ηλεκτρονίων από το ιόν αλογονιδίου. Αυτό οδηγεί στο σχηματισμό ενός ίζημα αργύρου αλογονιδίου, το οποίο είναι συχνά η κινητήρια δύναμη για την αντίδραση.
Παράγοντες που επηρεάζουν την αντιδραστικότητα:
* σταθερότητα Carbocation: Ο ρυθμός της αντίδρασης επηρεάζεται έντονα από τη σταθερότητα της καρβόλας που σχηματίζεται ως ενδιάμεσο. Οι πιο σταθερές καρβαμίες σχηματίζονται γρηγορότερα, οδηγώντας σε ένα πιο δραστικό αλκυλαλογονίδιο.
* Αφήνοντας την ομάδα ομάδας: Η ευκολία με την οποία το ιόν αλογονιδίου αφήνει το αλκυλαλογονίδιο επηρεάζει επίσης τον ρυθμό αντίδρασης. Το ιωδιούχο (Ι-) είναι η καλύτερη ομάδα αποχώρησης, ακολουθούμενη από βρωμίδιο (BR-), στη συνέχεια χλωριούχο (CL-) και φθορίου (F-) είναι το λιγότερο αποτελεσματικό.
σειρά αντιδραστικότητας:
Γενικά, η αντιδραστικότητα των κορεσμένων αλκυλαλογονιδίων προς Ag+ ακολουθεί αυτή τη σειρά:
Tertiary> δευτεροβάθμια> πρωτογενή
Επεξήγηση:
* Τριτοβάθμια αλκυλαλογονίδια: Οι τριτοβάθμιες καρβοσκώσεις είναι οι πιο σταθερές λόγω της επίδρασης των τριών αλκυλομάδων που περιβάλλουν το θετικό φορτίο. Αυτό καθιστά τα τριτογενείς αλκυλαλογονίδια το πιο αντιδραστικό προς το Ag+.
* Δευτερογενείς αλκυλαλογονίδια: Οι δευτερεύουσες καρβαμίες είναι λιγότερο σταθερές από τις τριτοβάθμιες καρβοσκώσεις επειδή έχουν λιγότερες αλκυλικές ομάδες που δωρίζουν πυκνότητα ηλεκτρονίων. Αυτό καθιστά τα δευτερογενή αλκυλαλογονίδια λιγότερο αντιδραστικά από τα τριτογενή αλκυλαλογιά.
* Πρωτογενή αλκυλαλογία: Οι πρωτογενείς καρφοσπώσεις είναι οι λιγότερο σταθερές, καθώς έχουν μόνο μία αλκυλική ομάδα που δωρίζει πυκνότητα ηλεκτρονίων. Επομένως, τα πρωτογενή αλκυλαλογιά είναι τα λιγότερο αντιδραστικά προς το Ag+.
Παράδειγμα:
* Το βρωμίδιο τριτ-βουτυλίου (τριτοβάθμια) θα αντιδρούσε ταχύτερα με το Ag+
* Το ισοπροπυλικό βρωμιούχο (δευτερογενές) θα αντιδρούσε βραδύτερα από το βρωμίδιο τριτ-βουτυλίου
* Το βρωμίδιο μεθυλίου (πρωτεύουσα) θα αντιδρούσε το πιο αργό.
Σημαντική σημείωση:
Η αντίδραση με Ag+ χρησιμοποιείται συχνά ως δοκιμή για την παρουσία αλκυλαλογονιδίων. Εάν σχηματίζεται ένα ίζημα (συνήθως ένα λευκό ή κίτρινο στερεό), υποδεικνύει την παρουσία αλκυλαλογονιδίου. Ωστόσο, η αντίδραση δεν είναι πάντοτε αξιόπιστη για την πρόβλεψη της ακριβούς τάξης της αντιδραστικότητας, καθώς άλλοι παράγοντες όπως η στερεοχημική παρεμπόδιση μπορούν επίσης να διαδραματίσουν κάποιο ρόλο.