Όταν μια μικρή ποσότητα υδροχλωρικού προστίθεται στο διάλυμα Na2HPO4 Το ρΗ το δεν αλλάζει;
Η κατάσταση
* na₂hpo₄ είναι το φωσφορικό υδρογόνο Disodium, ένα άλας που σχηματίζει ένα αδύναμο διάλυμα βάσης στο νερό.
* hcl είναι ένα ισχυρό οξύ.
Τι συμβαίνει
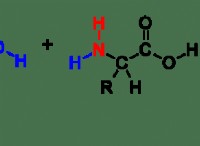
Όταν προσθέτετε μια μικρή ποσότητα HCl σε ένα διάλυμα Na₂hpo₄, συμβαίνει η ακόλουθη αντίδραση:
`` `
Hcl + na₂hpo₄ → naCl + nah₂po₄
`` `
* H⁺ ιόντα από HCl αντιδρά με hpo₄2 ⁻ ιόντα από na₂hpo₄ για να σχηματίσει h₂po₄⁻ ιόντα .
αλλαγή pH
Δεν είναι αλήθεια ότι το pH δεν αλλάζει καθόλου. Το pH θα μετατοπιστεί ελαφρώς * προς ένα πιο όξινο εύρος.
* na₂hpo₄ ενεργεί ως buffer. Αυτό σημαίνει ότι αντιστέκεται σε σημαντικές αλλαγές στο pH. Μπορεί να εξουδετερώσει μικρές ποσότητες προστιθέμενου οξέος (HCl σε αυτή την περίπτωση) μετατρέποντας το HPO₄2⁻ σε H₂po₄⁻.
* Η αλλαγή στο pH είναι μικρή Επειδή το h₂po₄⁻ είναι επίσης ένα αδύναμο οξύ. Το σύστημα buffer βοηθά στη διατήρηση ενός σχετικά σταθερού ρΗ.
Βασικά σημεία
* Χωρητικότητα buffering: Η ποσότητα οξέος ή βάσης που μπορεί να προστεθεί πριν από μια σημαντική μεταβολή του ρΗ εξαρτάται από τη συγκέντρωση του ρυθμιστικού διαλύματος.
* Η αλλαγή pH δεν είναι μηδενική: Μια μικρή αλλαγή στο pH θα εξακολουθεί να εμφανίζεται.
Συμπερασματικά, προσθέτοντας μια μικρή ποσότητα HCl σε ένα διάλυμα Na₂hpo₄ προκαλεί ελαφρά μείωση του ρΗ, αλλά το αποτέλεσμα ελαχιστοποιείται λόγω της προσωρινής δράσης του διαλύματος Na₂hpo₄.