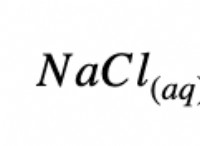Πόσα στοιχεία χρησιμοποιούνται για να συνθέτουν εκατομμύρια ενώσεις;
Εδώ είναι γιατί:
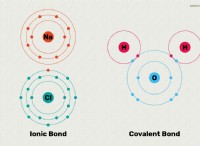
* Ο περιοδικός πίνακας διατηρεί περίπου 118 γνωστά στοιχεία. Αυτά τα στοιχεία χρησιμεύουν ως δομικά στοιχεία για όλα τα ύλη.
* Στοιχεία συνδυάζονται σε διαφορετικές αναλογίες και ρυθμίσεις. Αυτό επιτρέπει έναν τεράστιο αριθμό πιθανών συνδυασμών. Για παράδειγμα, μόνο δύο στοιχεία, ο άνθρακας και το υδρογόνο, μπορούν να σχηματίσουν αμέτρητους υδρογονάνθρακες.
* Χημικοί δεσμοί: Τα στοιχεία μπορούν να σχηματίσουν ενιαία, διπλά ή τριπλά ομόλογα μεταξύ τους, αυξάνοντας περαιτέρω τους πιθανούς συνδυασμούς.
* Ισομερή: Ακόμη και με τα ίδια στοιχεία, οι ενώσεις μπορούν να έχουν διαφορετικές δομικές ρυθμίσεις (ισομερή), οδηγώντας σε μοναδικές ιδιότητες.
Ενώ δεν μπορούμε να πούμε ακριβώς πόσες ενώσεις είναι δυνατές, είναι ασφαλές να πούμε ότι ο αριθμός είναι τεράστια και ενδεχομένως άπειρα, δεδομένου ότι τα απεριόριστα τρόπους μπορούν να συνδυαστούν.